药理学/氨基甙类抗生素
| 医学电子书 >> 《药理学》 >> 氨基甙类抗生素及多粘菌素 >> 氨基甙类抗生素 |
| 药理学 |
|
|
|
氨基甙类抗生素(aminoglycosides)都由氨基糖分子和非糖部分的甙元结合而成,它包括链霉素、庆大霉素、卡那霉素、西索米星以及人工半合成的妥布霉素、阿米卡星、奈替米星等。
一、氨基甙类抗生素的共性
氨基甙类抗生素的化学结构基本相似,因此具有共同特点,如水溶性好,性质稳定;此外,在抗菌谱,抗菌机制,血清蛋白结合率,胃肠吸收,经肾排泄,及不良反应等方面也有共性。
【抗菌作用】氨基甙类对各种需氧革兰阴性菌如大肠杆菌、克雷伯菌属、肠杆菌属、变形杆菌属等具高度抗菌活性。此外,对沙雷菌属、产碱杆菌属、布氏杆菌、沙门菌、痢疾杆菌、嗜血杆菌及分枝杆菌也具有抗菌作用。氨基甙类对革兰阴性球菌如淋球菌、脑膜炎球菌的作用较差。流感杆菌及肺炎支原体呈中度敏感,但临床疗效不显著。绿脓杆菌只对庆大霉素、阿米卡星、妥布霉素敏感,其中以妥布霉素为最强。对各型链球菌的作用微弱,肠球菌对之多属耐药,但金葡菌包括耐青霉素菌株对之甚为敏感。结核杆菌对链霉素、卡那霉素、阿米卡星和庆大霉素均敏感,但后者在治疗剂量时不能达到有效抑菌浓度。
按相同重量比较,庆大霉素和西索米星的抗菌活性较卡那霉素、妥布霉素、奈替米星和阿米卡星稍强,但临床用量中它们的抗菌作用并无明显差别。
【抗菌作用机制】氨基甙类的抗菌作用机制是阻碍细菌蛋白质的合成 。许多基本成分如活化氨基酸,转运核糖核酸(tRNA),信息核糖核酸(mRNA),酶Mg2+,始动因子(F1,F2,F3),ATP,GTP等都参与了蛋白质合成(图40-1)。
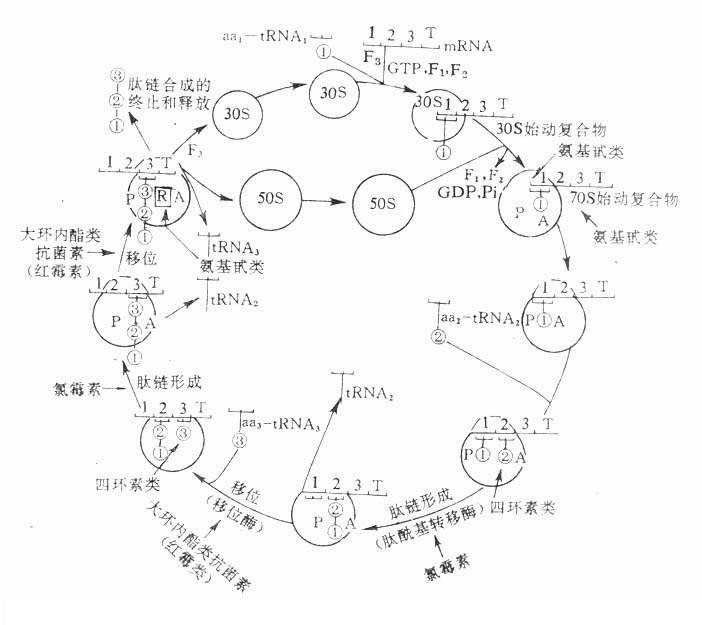
图40-1 核蛋白体循环及有关抗生素作用部位图解
30s、50s表示组成核蛋白体的两个亚基;A、P分别表示A位、P位,F1,F2,F3,为始动因子;R表示终止因子;aa1、aa2、aa3-tRNA表示tRNA1、2、3 携带三种不同的活化氨基酸;┗┷┛表示tRNA 上面三个小点表示反密码,它能翻译mRNA上相应的密码;mRNA上的1、2、3、T表示四个密码,T为终止密码,即停止合成的密码,T前可能有许多密码,为图示简便,仅顺序标出在T前的三个密码。每个密码包括三个核苷酸,称为三联密码。
细菌蛋白质合成分为三个阶段:①起始阶段 30S亚基与新生成的mRNA结合成mRNA-30S复合物,然后接上第一个氨基酰-tRNA(即甲酰蛋氨酰-tRNA),接在相当于50S的P位,称为30S起始复合物,后者很快与50S亚基结合成70S起始复合物。②肽链延长阶段 新的氨基酰-tRNA按mRNA的密码要求进入核蛋白体50S亚基的A位上,此时P位上的甲酰蛋氨酰或以后合成的肽链经肽酰转移酶的作用,基羧基与A位新接上的氨基酸的氨基结合而形成肽链。此时,在P位上的tRNA被释放回到细胞质内转运其他相应的氨基酸,核蛋白体30S亚基上的mRNA发生移位,把带有肽链的tRNA从A位移至P位。空出的A位又接受新的氨基酰-tRNA,如此反复使肽链不断延长。③终止阶段mRNA上出现终止信号时,表示蛋白质合成已结束,此时释放因子(R)进入A位,使肽链释放,tRNA及mRNA与核蛋白体分离,核蛋白体70S又解离为30S与50S亚基,重新参与蛋白质合成。
氨基甙类能影响蛋白质合成的许多环节:①起始阶段,抑制70S始动复合物的形成,②选择性地与30S亚基上靶蛋白结合(如P10),使mRNA上的密码错译,导致异常的、无功能的蛋白质合成;③阻碍终止因子(R)与核蛋白体A位结合,使已合成的肽链不能释放并阻止70S核蛋白体的解离,最终造成菌体内核蛋白体的耗竭。此外,氨基甙类通过离子吸附作用附着于细菌体表面造成胞膜缺损致使胞膜通透性增加,细胞内钾离子、腺嘌呤核苷酸、酶等重要物质外漏,从而导致细菌死亡。氨基甙类与β内酰胺类都是杀菌药,但它与后者不同,对静止期细菌有较强的作用。
【体内过程】氨基甙类在胃肠道不吸收或极少吸收(<1%)。口服后血药浓度很低,可用于胃肠道消毒,但在肾功能损害时,多次口服或直肠内给药,血药浓度可蓄积至中毒水平。肌内注射后氨基甙类吸收迅速且完全。30~90分钟达到峰浓度。常用的氨基甙类药代动力学参数见表40-1。氨基甙类静脉内给药,其浓度高低随剂量而异,一般在静脉滴注20~30分钟后,血浆中浓度与肌内注射者相同,本类药物中除链霉素外,与血浆蛋白很少结合。药物主要分布于细胞外液,组织与细胞内药物含量较低,分布容积大致与细胞外液容积相当,成人为15L(0.56L/kg)。肾脏皮质内药物浓度可超过血药浓度10~50倍。消除t1/2平均可达112~693小时。肾脏皮质内药物蓄积浓度越高,对肾毒性越大。氨基甙类可进入内耳外淋巴液,浓度与用药量成正比,其t1/2较血浆t1/2长5~6倍(图40-2)。当肾功能减退(无尿)时其浓度与t1/2均明显增加。氨基甙类在体内不被代谢,约90%以原形经肾小球过滤排出,尿药浓度极高,约为血浆峰浓度的25~100倍。
表40-1 常用氨基甙类的药代动力学
| 抗生素 | IM. 血药浓度达 峰时间(小时) |
t1/2(小时) | 24小时尿 排出(%) |
蛋白结合率 (%) |
|
| 正常 | 无尿 | ||||
| 链霉素 | 0.5~1.5 | 2.0~3.0 | 50~110 | 80 | 35 |
| 庆大霉素 | 0.75~1.0 | 1.7~2.3 | 48~72 | 70~80 | <10 |
| 妥布霉素 | 0.33~0.75 | 2.0~2.8 | 56~60 | 80~90 | <10 |
| 卡那霉素 | 0.75~1.0 | 2.1~2.4 | 60~90 | 84~90 | 0 |
| 阿米卡星 | 0.75~2.0 | 2.2~2.5 | 56~150 | 81~98 | 4.0 |
| 西索米星 | 0.75~1.0 | 2.0~2.3 | 35~37 | 85~87 | 0 |
| 奈替米星 | 0.5~1.0 | 2.2 | 33 | 80~90 | <10 |
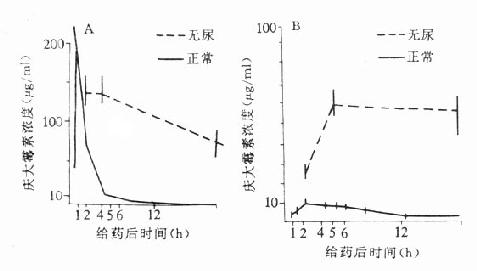
图40-2 正常和无尿豚鼠庆大霉素皮下注射50mg/kg后
血清(A)和外淋巴液(B)的药动学
庆大霉素浓度用生物测定法,每点为6只动物的均值,
无尿动物于给药前3小时切除肾脏
【不良反应】
1.耳毒性 临床反应可分为二类:一为前庭功能损害,有眩晕、恶心、呕吐、眼球震颤和平衡障碍,其发生率依次为:新霉素(已少用)>卡那霉素>链霉素>西索米星>庆大霉素>妥布霉素>奈替米星。另一为耳蜗神经损害,表现为听力减退或耳聋,其发生率依次为:新霉素>卡那霉素>阿米卡星>西索米星>庆大霉素>妥布霉素>链霉素。必须指出耳聋性的许多自觉症状并不明显,但经仪器监测显示有前庭功能或听力损害的“亚临床耳毒性”反应的发生率则可达10%~20%,最先影响为高频听力,随后逐渐波及低频部分。耳毒性发生机制可能是内耳淋巴液中药物浓度过高,损害内耳柯蒂氏器内、外毛细胞的糖代谢和能量利用,导致内耳毛细胞膜上钾钠离子泵发生障碍,终使毛细胞的功能受损。
为防止和减少耳毒性反应,在治疗过程中应注意观察耳鸣、眩晕等早期症状的出现,进行听力监测,并根据患者的肾功能(肌酐清除率等)及血药浓度来调整用药剂量。除非必要,应避免与高效利尿药或其他耳毒性药物合用。
2.肾毒性 氨基甙类主要经肾排泄并在肾(尤其是皮质部)蓄积,主要损害近曲小管上皮细胞,但不影响肾小球,临床化验可见蛋白尿、管形尿、尿中红细胞、肾小球过滤减少,严重者可发生氮质血症及无尿等。年老、剂量过高以及与其他肾毒性药物如呋塞米、多粘菌素、两性霉素B等合用时容易发生肾功能损害,在常用剂量时各药对肾的毒性顺序为:新霉素>卡那霉素>妥布霉素>链霉素,奈替米星肾毒性很低。
3.神经肌肉阻断作用 各种氨基甙类抗生素均可引起神经肌肉麻痹作用,虽较小见,但有潜在性危险。神经肌肉阻断作用与剂量及给药途径有关,如静脉滴注速度过快或同时应用肌肉松弛剂与全身麻醉药。重症肌无力者尤易发生,可致呼吸停止。其机制是乙酰胆碱的释放需Ca2+的参与,药物能与突触前膜上“钙结合部位”结合,从而阻止乙酰胆碱释放。当出现神经肌肉麻痹时,可用钙剂或新斯的明治疗。
4.过敏反应 氨基甙类可以引起嗜酸粒细胞增多,各种皮疹,发热等过敏症状,也可引起严重过敏休克,尤其是链霉素引起的过敏休克发生率仅次于青霉素G,应引起警惕。
二、各种氨基甙类抗生素药理特点及应用
1.链霉素(streptomycin)是由链丝菌培养液提取而得,常用其硫酸盐,性质稳定,水溶液在室温可保持一周。口服不吸收,肌肉注射吸收快,30~60分钟达峰浓度,t1/2为2~3小时,一次注射有效浓度可达6~8小时,年龄超过40岁t1/2可延长至9小时,主要分布于细胞外液,大部分经肾排泄,肾功不全时,排泄减慢。
链霉素对多数革兰阴性菌有强大抗菌作用,但因毒性与耐药性问题,限制了它的临床应用。目前临床主要用于:①鼠疫与兔热病,对此链霉素是首选药;②布氏杆菌病,链霉素与四环素合用也有满意的效果;③感染性心内膜炎,对草绿色链球菌引起者,以青霉素合并链霉素为首选;对肠球菌引起者,也需青、链合用治疗,但部分菌株对链霉素耐药,可改用庆大霉素或妥布霉素等;④结核病,链霉素为最早的抗结核药,现仍有应用,但必须与其他抗结核药联合应用,以延缓耐药性的发生;⑤链霉素与青霉素或氨苄西林合用,可用于预防常发的细菌性心内膜炎及呼吸、胃肠道及泌尿系统手术后感染。
链霉素治疗时常可出现头痛、头晕、呕吐、耳鸣、平衡失调和眼球震颤。多是可逆的。严重者可致永久性耳聋。对肾脏的毒性为氨基甙类中最轻者,但肾功能不全者仍应慎用。
2.庆大霉素(gentamicin)是目前临床最为常用的广谱氨基甙类。庆大霉素水溶液稳定,水针剂常作肌内或静脉滴注给药。体内过程与链霉素相仿(表40~1)。但其有效与安全的血药浓度较低(4~8mg/L)。药物主要经肾排泄,部分经胆汁入肠,胆汁药物浓度可达血药浓度的60%~80%,t1/2约3小时。
庆大霉素广泛用于治疗敏感菌的感染:①严重革兰阴性杆菌的感染如败血症、骨髓炎、肺炎、腹膜感染、脑膜炎等、庆大霉素是首选药;②绿脓杆菌感染,庆大霉素常与羧苄西林合用可获协同作用,但两药不可同时混合滴注,因后者可使本药的活力降低;③病因未明的革兰阴性杆菌混合感染,庆大霉素与广谱半合成青霉素类(羧苄西林或哌拉西林等)或头孢菌素联合应用可以提高疗效;④与青霉素联合治疗肠球菌心内膜炎;与羧苄西林、氯霉素联合治疗革兰阴性杆菌心内膜炎;⑤庆大霉素口服可用于肠道感染或肠道术前准备;⑥庆大霉素局部用于皮肤、粘膜表面感染、眼、耳、鼻部感染,但因可致光敏感反应,大面积应用易致吸收毒性,故少作局部应用。
不良反应有前庭神经功能损害,但较链霉素少见,对肾脏毒性则较多见。
3.卡那霉素(kanamycin)由链丝菌培养液获得。卡那霉素体内过程与链霉素、庆大霉素基本相同。其抗菌谱与链霉素相似,但稍强,对多数常见的革兰阴性菌及结核菌有效,但对绿脓杆菌无效。体内抗菌有效的血药浓度范围为8~16µg/ml。卡那霉素由于毒性及耐药菌较多见,其在临床应用已为庆大霉素等其他氨基甙类药所取代。
4.妥布霉素(tobramycin)由链丝菌培养液中提得,也可由卡那霉素B脱氧而成,其水溶液非常稳定。
抗菌作用与庆大霉素相似,对绝大多数肠杆菌科细菌、绿脓杆菌及葡萄球菌具良好的抗菌作用。最突出的是对绿脓杆菌作用较庆大霉素强2~4倍,并且对庆大霉素耐药者仍有效,对肠球菌及除绿脓杆菌外的假单孢菌属及厌氧菌无效,对肺炎杆菌、肠杆菌属与变形杆菌属的作用较庆大霉素略强;但对沙雷菌和沙门菌的作用略差。
妥布霉素与庆大霉素相同,主要用于各种严重的革兰阴性杆菌感染,但一般不作为首选药。对绿脓杆菌感染或需较长时间用药者,如感染性心内膜炎,以选用妥布霉素为宜。
妥布霉素的耳毒性较庆大霉素略低,但仍应警惕。一般每日剂量不宜超过5mg/kg,血药浓度不宜超过12mg/L。在肾功能减退时还应根据血清肌酐清除率,调整剂量与给药间隔。
5.阿米卡星(amikacin,丁胺卡那霉素)是卡那霉素的半合成衍生物,其抗菌谱为本类药物中最宽的。其突出优点是对许多肠道革兰阴性菌和绿脓杆菌所产生的钝化酶稳定,因而主要用于治疗对其他氨基甙类耐药菌株(包括绿脓杆菌)所致的感染,如对庆大霉素、卡那霉素耐药株引起的尿路、肺部感染,以及绿脓、变形杆菌所致的败血症。与羧苄西林或头孢噻吩合用。连续静脉滴注治疗中性粒细胞减少或其他免疫缺陷者感染,可获得满意效果。阿米卡星仅可为革兰阴性菌所产生的一种乙酰转移酶AAC(b')所钝化而耐药,此外,由于细胞壁屏障作用,致使药物不能有效渗入细菌体也可导致耐药株产生。
6.西索米星(sisomicin)由小单孢菌发酵液中获得,药用其硫酸盐,易溶于水。抗菌谱及体内过程与庆大霉素很相似,抗绿脓杆菌作用比庆大霉素强两倍,对金葡菌、克雷伯菌属、球菌属、大肠杆菌、变形杆菌和化脓性球菌也有良效。临床上用于上述细菌引起的感染。毒性约比庆大霉素大两倍。
7.奈替米星(netilmicin)是新的氨基甙类抗生素。其药动学特性与庆大霉素、妥布霉素相似,它也像阿米卡星不被大多数钝化酶灭活。对一些革兰阴性杆菌,如大肠杆菌、克雷伯杆菌、沙雷杆菌、各型变形杆菌和绿脓杆菌都具有较强抗菌活性,对流感嗜血杆菌、沙门菌、志贺菌和奈瑟菌也有效。对某些耐其他氨基甙类的革兰阴性杆菌及耐青霉素类的金葡菌也有效。适用于尿路、肠道、呼吸道、皮肤软组织、骨和关节、腹腔及创口部分的感染。奈替米星的耳、肾毒性是氨基甙类抗生素中最低者。但仍宜注意。
8.新霉素(neomycin)抗菌谱似卡那霉素。肌内注射吸收快,毒性比卡那霉素大,易引起永久性耳聋和肾损害,不宜注射给药。口服很少吸收,毒性较小,可用于肠道感染和肠道消毒。局部外用治疗皮肤粘膜浅表感染。
【附】:大观霉素(spectinomycin)由链霉菌所产生的一种氨基环醇类(aminocyclitols)抗生素,主要对淋球菌有高度抗菌活性,6.3mg/L可抑制大多数淋球菌。肌注2g,1小时血药浓度达峰100mg/L,t1/2约2.5小时。药物主要经尿排泄。临床的唯一适应证是无并发症的淋病,限于对青霉素、四环素等耐药的淋病或患者对青霉素过敏者。
三、药物相互作用
氨基甙类与两性霉素、杆菌肽、头孢噻吩、多粘菌素或万古霉素合用能增加肾脏毒性。呋塞米(速尿)、利尿酸及甘露醇等能增加氨基甙类的耳毒性。苯海拉明、敏可静、安其敏等抗组胺药可掩盖氨基甙类的耳毒性。氨基甙类能增强骨骼肌松弛药及全身麻醉药引起的肌肉松弛作用,可导致呼吸抑制。
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 关于“药理学/氨基甙类抗生素”的留言: | |
|
目前暂无留言 | |
| 添加留言 | |