糖原
| A+医学百科 >> 糖原 |
糖原(glycogen)(C6H10O5)n又称肝糖,动物淀粉,由葡萄糖结合而成的支链多糖,其糖苷链为α型。动物的贮备多糖。哺乳动物体内,糖原主要存在于骨骼肌(约占整个身体的糖原的2/3)和肝脏(约占1/3)中,其他大部分组织中,如心肌、肾脏、脑等,也含有少量糖原。低等动物和某些微生物(如:真菌、酵母)中,也含有糖原或糖原类似物。
目录 |
简介
糖原贮藏于肝细胞及肌细胞浆中,其形状为大小不等的颗粒,遇碘则变褐色,易溶于水,机体坏死后,糖原即受到破坏,因此须采取新鲜标本,并及时固定。糖原不等于糖类,只是糖类的一种。糖类从组织化学技术的角度分类与生物化学的分类并非一致。从组织化学的角度,糖类可略分为多糖、中性糖液物质和酸性粘液物质及粘蛋白和粘脂质。多糖主指糖原,是由许多葡萄糖分子以糖苷键组成的聚合体。当机体死亡,即很快分解为葡萄糖。
动物和细菌细胞内贮存的多糖,完全由葡萄糖组成。在动物体内以肝脏和骨骼肌中储量最丰富,与淀粉在植物中的作用相当。糖原在体内酶促作用下的合成和分解可维持血糖正常水平,细菌中糖原用于供能和供碳。干燥状态下为白色无定形粉末,无臭,有甜味。与碘显棕红色,在430-490nm下呈现最大光吸收。部分溶于水而成胶体溶液,不溶于乙醇。结构与支链淀粉相似,主要是α-D-葡萄糖,按α(1→4)糖苷键缩合失水而成,另有一部分支链通过α(1→6)糖苷键连接。用细算后淀粉酶水解时生成麦芽糖和葡萄糖。可用30%氢氧化钠处理动物肝脏,再加乙醇沉淀制备。
糖原,是动物的糖贮存库,也可看做体内能源库。糖原的结构与支链淀粉有基本相同的结构(葡萄糖单位的分支链),只是糖原的分支更多。糖原呈无定形无色粉末,较易溶于热水,形成胶体溶液。糖在动物的肝脏和肌肉中含量最大,当动物血液中葡萄糖含量较高时,就会结合成糖原储存于肝脏中。当葡萄糖含量降低时,糖原就可分解成葡萄糖而供给机体能量。Glycogen(糖原),不含DNase,不含RNase,可以用作沉淀DNA或RNA的辅助沉淀剂。
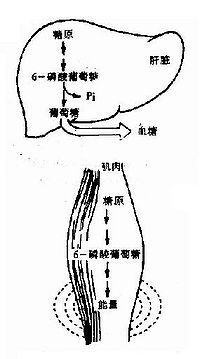
糖原是由葡萄糖残基构成的含许多分支的大分子高聚物。分子量一般在106-107道尔顿,可高达108道尔顿,是体内糖的贮存形式,分子中葡萄糖主要以α-1,4-糖苷键相连形成直链,其中部分以α-1,6-糖苷键相连构成枝链,糖原主要贮存在肌肉和肝脏中,肌肉中糖原约占肌肉总重量的1-2%,肝脏中糖原占总量6-8%。肌糖原分解为肌肉自身收缩供给能量,肝糖原分解主要维持血糖浓度。
糖原是由多个葡萄糖组成的带分枝的大分子多糖,分子量一般在106-107道尔顿,可高达108道尔顿,是体内糖的贮存形式,分子中葡萄糖主要以α-1,4-糖苷键相连形成直链,其中部分以α-1,6-糖苷键相连构成枝链,糖原主要贮存在肌肉和肝脏中,肌肉中糖原约占肌肉总重量的1-2%约为400克,肝脏中糖原占总量6-8%约为100克。肌糖原分解为肌肉自身收缩供给能量,肝糖原分解主要维持血糖浓度。
植物及动物(消化道中)的淀粉酶均能作用于糖原,产生麦芽糖及糊精。在活细胞内,糖原的降解是从非还原性末端开始,逐个切下葡萄糖基,生成D-葡萄糖-1-磷酸,再通过糖酵解等途径进一步分解产生能量和提供合成其他生物分子所需要的碳架。由于高度的分支状构造,使得糖原分子中约8~10%的葡萄糖处于可被利用的非还原末端,这就便于在需要时可短时间内快速大量动用,不需要时快速恢复贮存。例如:肌肉收缩运动时,所需要的以ATP形式提供的能量,为静止时的几千至几万倍,这些ATP主要依赖糖原的分解来提供。葡萄糖、乳酸、脂肪酸、甘油,某些氨基酸都可以通过适当的代谢途径转变为贮存的糖原;体内由葡萄糖合成糖原的过程称为糖原生成作用,由非糖物质生成葡萄糖或糖原的过程称为糖异生作用。
人体内糖原的贮存或消耗是一个受激素及底物控制的过程。通过调节参加合成及降解过程的酶的活性,机体的糖原代谢和血糖水准得到恰当的控制。糖原的不正常代谢,表现为糖原蓄积症,其原因常是由于缺乏有关的酶。例如,葡萄糖-6-磷酸酶缺乏的患者,肝及肾含有较多量结构正常的糖原,临床症状为肝肿大、极度低血糖、高脂血、高尿酸血、酮中毒以及生长停滞等。
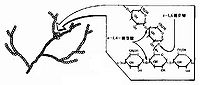
分子结构
糖原的分子结构与支链淀粉相似。主要由D-葡萄糖通过α-1,4联接组成糖链,并通过α-1,6连接产生支链。糖原分子中分支比支链淀粉更多,平均每间隔12个α-1,4联接的葡萄糖就是一个分支点(支链淀粉分子中平均间隔约为20~25个葡萄糖)。分子量范围从几百万至几千万。提纯的糖原为白色无定形颗粒,还原性极弱,易溶于水而产生乳白色胶体溶液,比旋约为+200°,对碱耐受性比较强,与碘反应呈红棕色,在醇中溶解度小,加乙醇于水溶液中可使糖原沉淀析出。
基本原理
糖原由D-葡萄糖的分支或直链组成,在肝和肌肉最丰富。过碘酸是一种强氧化剂,能将葡萄糖中乙二醇基(CHOH-CHOH)氧化成二个游离醛基(—CHO),游离醛基与Schiff's试剂反应生成紫红色产物,颜色深浅与多糖含量成正比。由于单糖在固定、脱水和包埋等组织化学操作过程中被抽提掉,故一般组织标本上所能显示的糖类主要是多糖,包括糖原、粘多糖、粘蛋白、糖蛋白和糖脂等。因此要确定此红色物质是否糖原还需要同时进行对照实验。糖原可被唾液淀粉酶水解,先用唾液淀粉酶作用再进行PAS显色,若反应为阴性,则表明是糖原,反之则为其他多糖。
糖原的合成
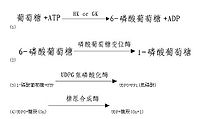
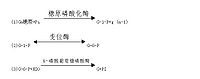
由葡萄糖(包括少量果糖和半乳糖)合成糖原的过程称为糖原合成,反应在细胞质中进行,需要消耗ATP和UTP,合成反应包括以下几个步骤:
糖原合成酶催化的糖原合成反应不能从头开始合成第一个糖分子,需要至少含4个葡萄糖残基的α-1,4-多聚葡萄糖作为引物(primer),在其非还原性末端与UDPG反应,UDPG上的葡萄糖基C1与糖原分子非还原末端C4形成α-1,4-糖苷链,使糖原增加一个葡萄糖单位,UDPG是活泼葡萄糖基的供体,其生成过程中消耗UTP,故糖原合成是耗能过程,糖原合成酶只能促成α-1,4-糖苷键,因此该酶催化反应生成为α-1,4-糖苷键相连构成的直链多糖分子如淀粉。
机体内存在一种特殊蛋白质称为glycogenin,可做为葡萄糖基的受体,从头开始如合成第一个糖原分子的葡萄糖,催化此反应的酶是糖原起始合成酶(glycogen initiaor synthase),进而合成一寡糖链作为引物,再继续由糖原合成酶催化合成糖。同时糖原分枝链的生成需分枝酶(branching enzyme)催化,将5-8个葡萄糖残基寡糖直链转到另一糖原子上以α-1.6-糖苷键相连,生成分枝糖链,在其非还原性末端可继续由糖原合成酶催化进行糖链的延长。多分枝增加糖原水溶性有利于其贮存,同时在糖原分解时可从多个非还原性末端同时开始,提高分解速度。
糖原的分解
糖原分解不是糖原合成的逆反应,除磷酸葡萄糖变位酶外,其它酶均不一样,反应包括:
这样将糖原中1个糖基转变为1分子葡萄糖,但是磷酸化酶只作用于糖原上的α(1→4)糖苷键,并且催化至距α(1→6)糖苷键4个葡萄糖残基时就不再起作用,这时就要有脱枝酶(debranching enzyme)的参与才可将糖原完全分解。脱枝酶是一种双功能酶,它催化糖原脱枝的两个反应,第一种功能是4-α-葡聚糖基转移酶(4-α-D-glucanotrnsferase)活性,即将糖原上四葡聚糖分枝链上的三葡聚糖基转移到酶蛋白上,然后再交给同一糖原分子或相邻糖原分子末端具自由4羟基的葡萄糖残基上,生成α(1→4)糖苷键,结果直链延长3个葡萄糖(图5-6),而α(1→6)分枝处只留下1个葡萄糖残基,在脱枝酶的另一功能,即1,6-葡萄糖苷酶活性催化下,这个葡萄糖基被水解脱下,为游离的葡萄糖,在磷酸化酶与脱枝酶的协同和反复的作用下,糖原可以完全磷酸化和水解。
糖原代谢的调节
糖原代谢的别构调节
6-磷酸葡萄糖可激活糖原合成酶,刺激糖原合成,同时,抑制糖原磷酸化酶阻止糖原分解,ATP和葡萄糖也是糖原磷酸化酶抑制剂,高浓度AMP可激活无活性的糖原磷酸化酶b使之产生活性,加速糖原分解。Ca2+可激活磷酸化酶激酶进而激活磷酸化酶,促进糖原分解。
激素的调节
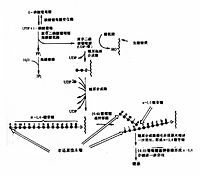
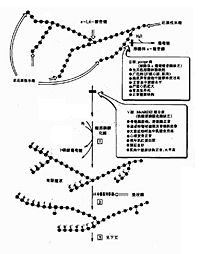
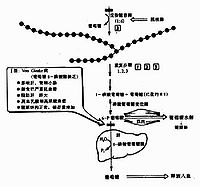
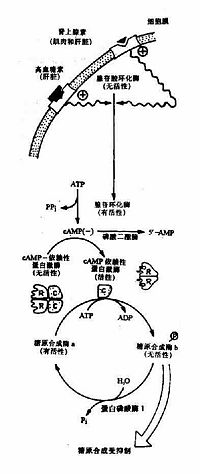
体内肾上腺素和胰高血糖素可通过cAMP连锁酶促反应逐级放大,构成一个调节糖原合成与分解的控制系统。
当机体受到某些因素影响,如血糖浓度下降和剧烈活动时,促进肾上腺素和胰高血糖素分泌增加,这两种激素与肝或肌肉等组织细胞膜受体结合,由G蛋白介导活化腺苷酸环化酶,使cAMP生成增加,cAMP又使cAMP依赖蛋白激酶(cAMp dependent protein kinase)活化,活化的蛋白激酶一方面使有活性的糖原合成酶a磷酸化为无活性的糖原合成酶b(图4?9);另一面使无活性的磷酸化酶激酶磷酸化为有活性的磷酸化酶激酶,活化的磷酸化酶激酶进一步使无活性的糖原磷酸化酶b磷酸化转变为有活性的糖原磷酸化酶a(图4?0),最终结果是抑制糖原生成,促进糖原分解,使肝糖原分解为葡萄糖释放入血,使血糖浓度升高,肌糖原分解用于肌肉收缩。
糖原生成作用
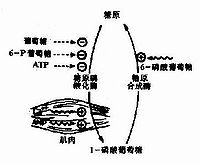
指生物体内由葡萄糖等单糖合成糖原的过程。为糖原分解的逆过程。将更普遍的用低分子的乳糖等通过糖酵解的逆过程而生成糖原的过程称糖异生以资与之区别。动物主要在肝脏或肌肉中进行,为能源储藏的一个主要过程。食物消化后由消化器官吸入血液中的葡萄糖,通过肝门脉而运到肝脏,在那里在已糖激酶和ATP的作用下先磷酸化成6-磷酸葡萄糖,再经1-磷酸葡萄糖而成UDP葡萄糖,再在糖原合成酶的作用下生成糖原。此时形成α-1,4-糖苷键,但其α-1,6键由称为脱支酶的一种转糖苷酶的协同作用下而形成。另外为了引起这一反应需要有少量的多糖(如糖原本身)作引子。此反应在酵母菌等微生物中也进行,在高等植物中的淀粉储藏和细菌的形成多糖等也与此类似。但因生物的不同,其酶及反应途径有些不同。动物及植物分别以葡萄糖和蔗糖为组织的能源及体液的重要组成分,组织的正常机能是在这些物质浓度水平的良好调节状态下进行的,而糖原合成在此调节作用中具有重要意义。
糖原的作用
糖类——碳水化合物,是人体最重要的供能物质,主要以葡萄糖的形式被吸收。葡萄糖迅速氧化,供应能量。糖类也是构成机体的重要原料,参予细胞的多种活动。例如糖类和蛋白质合成糖蛋白,是抗体、酶类和激素的成分。糖类与脂类合成糖脂。是细胞膜和神经组织的原料。糖类对维持功能有特别作用。糖类有解毒作用。肝糖原储备充足时,可增强抵抗力,食物供应足量糖类,可减少蛋白质作为供能的消耗。
肝脏是调节血糖浓度衡定的重要器官。肝脏原有糖原约占肝脏重量的5~6%,成人平均约有糖原100克左右。当长时间大量摄入糖类食物后,肝糖原可达150克左右,健康胖者甚至可达150~200克,当饥饿10余小时后,大部分肝糖原被消耗。
血糖过低或食欲消失时,可口服或静注葡萄糖。口服后葡萄糖经门脉吸收后直接入肝,较静脉输入更为有利。肝病患者若糖耐量降低,而血糖升高,有肝原性糖尿病时,则不宜静注葡萄糖,也不必口服葡萄糖。
肝病患者应供给足量糖类,以确保蛋白质和热量的需要,以促进肝细胞的修复和再生。肝内有足够糖原储存,可增强肝对感染和毒素的抵抗力,保护肝脏免遭进一步损伤,促进肝功能的恢复。但肝内糖原储存有一定限度,过多供给葡萄糖,也不能合成过多糖原,因此,强调限制热量过剩导致肥胖,对肝病是有着至关重要的作用。
强调食疗的意义在于此,针对自身疾病和营养情况选择补充食品,改善人体各器官的功能,各种食品都将对人体的某种器官发挥一定的作用。如果饮食得当则可维持生理平衡,一般认为,米、面、肉、蛋多属酸性食物,蔬菜、水果以碱性居多,适当调理有利于人体代谢的酸碱平衡。
肝病患者或兼有高血压、动脉硬化、肥胖的人应少食动物脂肪,食用肉类时宜用鱼、虾、瘦肉;平素兼有脾胃虚弱的人可多吃白扁豆和豆制品,因为这类食品区脾胃、除湿热,且富含蛋白质,可调节并增强消化系统的功能。了解每种食品的基本营养成分和性味作用,实现自我疗养的真正意义。
相关疾病
糖原累积病
简介
糖原累积病是一类由于先天性酶缺陷所造成的糖原代谢障碍疾病,多数属常染色体隐性遗传,发病因种族而异。根据欧洲资料,其发病率为 1/(2万~2.5万)。糖原合成和分解代谢中所必需的各种酶至少有8种,由于这些酶缺陷所造成的临床疾病有12型,其中Ⅰ、Ⅲ、Ⅳ、Ⅵ、Ⅸ型以肝脏病变为主;Ⅱ、Ⅴ、Ⅶ型以肌肉组织受损为主。这类疾病有一个共同的生化特征,即是糖原贮存异常,绝大多数是糖原在肝脏、肌肉、肾脏等组织中贮积量增加。仅少数病种的糖原贮积量正常,而糖原的分子结构异常。
病因
糖原是由葡萄糖单位构成的高分子多糖,主要贮存在肝和肌肉中作为备用能量,正常肝和肌肉分别含有约4%和2%糖原。摄人体内的葡萄糖在葡萄糖激酶、葡糖磷酸变位酶和尿苷二磷酸葡糖焦磷酸化酶的催化下形成尿苷二磷酸葡萄糖(UDPG)。然后由糖原合成酶将UDPG提供的葡萄糖分子以α-1,4-糖苷键连接成一个长链;每隔3~5个葡萄糖残基由分支酶将1,4位连接的葡萄糖转移成1,6位连接,形成分支,如是扩展,最终构成树状结构的大分子。糖原的分子量高达数百万以上,其最外层的葡萄糖直链较长,大多为10~15个葡萄糖单位。糖原的分解主要由磷酸化酶催化、从糖原分子中释放1-磷酸葡萄糖。但磷酸化酶的作用仅限于1,4糖苷键,并且当分枝点前仅存4个葡萄糖残基时就必须由脱枝酶(淀粉1,6-葡糖苷酶,amyol-1,6-glucosidase)将其中的三个残基转移至其他直链以保证磷酸化酶的作用继续进行。与此同时,脱枝酶可以解除α-l,6-糖苷键连接的一个葡萄糖分子,这样反复进行便保证了机体对葡萄糖的需求。存在于溶酶体中的α-1,4葡糖苷酶(酸性麦芽糖酶)也能水解不同长度的葡萄糖直链,使之成为麦芽糖等低聚糖分子。GSD是由于患者缺乏上述糖原合成和分解过程中任一酶的缺陷使糖原合成或分解发生障碍,导致糖原沉积于组织中而致病。由于酶缺陷的种类不同,造成多种类型的糖原代谢病,常见类型见表。其中Ⅰ、Ⅲ、Ⅵ、Ⅸ型以肝脏病变为主,Ⅱ、Ⅴ、Ⅶ型以肌肉组织受损为主。
症状诊断
该病系遗传性疾病,患儿出生时就有肝脏肿大。随着年龄的增长,出现明显低血糖症状,如软弱无力、出汗、呕吐、惊厥和昏迷,并可以出现酮症酸中毒。
患儿生长发育迟缓 ,智力无障碍,体型矮小、肥胖,皮肤颜色淡黄,腹部膨隆,肝脏显著增大,质地坚硬,肌肉发育差,无力,尤其以下肢最为显著。多数患此病症者不能存活至成年,往往死于酸中毒昏迷。轻症病例在成年后可以获得好转。目前本病可区分为十多个亚型,其中以Ⅰ型最为常见。
该病需与糖尿病相鉴别:
糖尿病患者也有酸中毒,低血糖的症状,但糖尿病患者有典型的症状是“三多一少”,即多饮、多尿、多食及消瘦,根据次症状可鉴别。
治疗
用高蛋白、高葡萄糖饮食,多次喂养,以维持血糖正常水平,尤应于午夜加餐1次,以避免次晨低血糖。其他治疗包括防止感染,纠正酸中毒(可用NaHCO3,禁用乳酸钠)。纠正低血糖后如果血脂仍继续升高,可用安妥明50mg/(kg.d)。高尿酸血症如采用饮食疗法不能控制时,可用别嘌呤醇5~10mg/(kg.d)。激素治疗有益于维持正常血糖水平、提高食欲。胰高血糖素、各种类固醇激素、甲状腺素对改善症状皆可有暂时的疗效。外科方法如作门-腔静脉吻合术,使肠吸收的葡萄糖越过肝,直接进入血循环,可能术后肝缩小,生长加速,但长期效果并不肯定。亦有报告作肝移植者,效果不明且不易推广。其他有采用酶替代治疗等,但效果并不佳。
糖原累积症Ⅳ型:糖原无特效疗法,高蛋白低糖饮食,加食玉米油未能阻止肝硬化进程。用纯化的葡萄糖素未能取得肯定效果。曲霉菌属提取物可使肝糖原急剧减少,因而是一个有研究前途的治疗方法。此外,可施行肝移植。
总之,对本症主要是饮食治疗和对症处理,使患儿能渡过婴幼儿期,因4岁后机体逐步适应其他代谢途径,临床症状可减轻。
1型糖原储存疾病
疾病特征:1型糖原储存疾病(GSD1)的疾病特征是肝脏肾脏糖原和脂肪的积聚,导致肝肿大和肾肿大。一些未接受治疗的新生儿有严重的低血糖;未接受治疗的新生儿更常见的症状是在3至4个月时出现的肝肿大、乳酸酸中毒、高尿酸血症、高脂血症和/或低血糖癫痫。患病儿童通常有两颊肥胖的娃娃脸,四肢相对细,身材短小和小腹突起。也可能出现黄瘤和腹泻。血小板功能障碍可能导致频繁鼻衄的出血倾向。未经治疗的GSDIb生命最初几年伴有中性粒细胞和单核细胞的功能障碍和慢性中性粒细胞减少症,这些都会导致复发性的细菌感染和口腔及肠粘膜溃疡。未经治疗的GSD1的长期并发症包括生长迟缓及其导致的身材矮小、骨质疏松、青春期推迟、痛风、肾脏疾病、肺动脉高血压、有恶化倾向的肝腺瘤、多囊卵巢、胰腺炎和脑功能变化。接受了治疗的儿童应该有正常生长和青春期。许多患者存活到成人期。
诊断/检测:GSD1的诊断是基于临床表征、异常的血液/血浆中葡萄糖、乳糖、尿酸、甘油三酯和脂类的浓度和分子遗传血检测的。G6PC基因(GSD1a)的突变导致了80%的GSD1;SLC37A4基因(GSD1b)的突变导致了20%的GSD1。对这两个基因的分子遗传学检测临床都有提供。
治疗:症状的治疗:医疗性的的营养疗法来保持正常的葡萄糖浓度,防止低血糖,也为生长发育提供最优化的营养。当食疗不能完全控制血中尿酸浓度,使用别嘌呤醇预防痛风;在有代谢控制情况下脂类水平仍升高应使用降低脂类药物;补充柠檬酸盐帮助预防发展出尿结石或改善肾钙质沉着;用血管紧张素转化酶(ACE)抑制剂治疗微白蛋白尿;治疗末期肾病采用肾移植;手术或其它干预,如皮下酒精注射和射频消蚀治疗肝腺瘤;对医疗措施不应的或同时有肝细胞癌的病人采取肝移植;用人类粒细胞集落刺激因子(G-CSF)治疗GSD1b的复发性感染。对并发症的预防:改善高尿酸血症和高脂血症保持正常肾功能预防肾脏疾病。监控: 十岁以后每年对肾脏和肝脏进行超声检查;发现肝腺瘤后每3-6个月进行肝脏超声检查。应避免的药剂/情况:饮食中果糖和蔗糖都应该是低量的;半乳糖和乳糖摄入量应该被限制在每天一剂量。高危血亲的检测:分子遗传血检测(如果家族特异突变已知)和/或出生后即由代谢医生进行评估(如果家族特异突变未知)可以帮助对GSD1的高危兄弟姐妹的早期诊断和治疗。
|
|||||||||||||||||||||||||||||||||||||||||||||||||||
| 关于“糖原”的留言: | |
|
目前暂无留言 | |
| 添加留言 | |