氰基
| A+医学百科 >> 氰基 |
[英]cyan
氰基(CN)中的碳原子和氮原子通过叁键相连接。这一叁键给予氰基以相当高的稳定性,使之在通常的化学反应中都以一个整体存在。因该基团具有和卤素类似的化学性质,常被称为拟卤素。通常为人所了解的氰化物都是无机氰化物,俗称山奈(来自英语音译“Cyanide”),是指包含有氰根离子(CN-)的无机盐,可认为是氢氰酸(HCN)的盐,常见的有氰化钾
和氰化钠。它们多有剧毒,故而为世人熟知。另有有机氰化物,是由氰基通过单键与另外的碳原子结合而成。视结合方式的不同,有机氰化物可分类为腈(C-CN)和异腈(C-NC),相应的,氰基可被称为腈基(-CN)或异腈基(-NC)。
氰化物拥有令人生畏的毒性,然而它们绝非化学家的创造,恰恰相反,它们广泛存在于自然界,尤其是生物界。氰化物可由某些细菌,真菌或藻类制造,并存在于相当多的食物与植物中。在植物中,氰化物通常与糖分子结合,并以含氰糖苷(cyanogenic glycoside)形式存在。比如,木薯中就含有含氰糖苷,在食用前必须设法将其除去(通常靠持续沸煮)。水果的核中通常含有氰化物或含氰糖苷。如杏仁中含有的苦杏仁苷,就是一种含氰糖苷,故食用杏仁前通常用温水浸泡以去毒。
在广义酸碱理论中,氰离子(CN-)被归类为软碱,故而可与软酸类的低价重金属离子形成较强的结合。基于此,氰化物
被广泛应用于湿法冶炼金、银。氰化物被大量用于黄金开采中,因为金单质由于氰离子的络合作用降低了其氧化电位从而能在碱性条件下被空气中的氧气氧化生成可溶性的金酸盐而溶解,由此可以有效地将金从矿渣中分离出来,然后再用活泼金属比如锌块经过置换反应把金从溶液中还原为金属(参见湿法冶金)。
目录 |
有机合成
氰化物在有机合成中是非常有用的试剂。常用来在分子中引入一个氰基,生成有机氰化物,即腈。例如纺织品中常见的腈纶,它的化学名称是聚丙烯腈
。腈通过水解可以生成羧酸;通过还原可以生成胺,等等。可以衍生出其它许多的官能团来。
其毒性跟CN离子对重金属离子的超强络合能力有关。CN 主要跟细胞色素P450中的金属离子结合,从而使其失去在呼吸链中起到的传递电子能力,进而使中毒者死亡。氰化物中毒一般都很迅速。临床上常用的抢救方法是用硫代硫酸钠溶液进行静脉注射,同时使那些尚有意识的病人吸入亚硝酸异戊酯进行血管扩张来克服缺氧。常见的氰化物中毒原因是误食含氰果仁儿,比如生桃仁儿等。
氰化物与欧洲环境灾难
继前苏联切尔诺贝利核污染之后,又一场巨大环境灾难降临在欧洲大地。今年的1月30日深夜至31日晨,罗马尼亚北部边境城镇奥拉迪亚,连续几天几夜的大雨使镇上乌鲁尔金矿用于生产黄金的氰化物废水漫过大坝向下游汹涌冲去。这股“死亡之水”所经之处,所有生物在极短的时间内暴亡,流经罗马尼亚、匈牙利和南联盟的欧洲大河之一蒂萨河及其支流内的80%鱼类已完全灭绝,而且这股毒水还流入了欧洲最著名的蓝色河流--多瑙河,使当地居民深感痛惜,他们在蒂萨河、多瑙河的多处大桥上插上一面面黑旗、燃着一支支蜡烛,无奈而又愤怒的一朵朵洁白的小花投到河里,为河流的“死亡”而默默地哀悼。
氰化物废水何以造成如此巨大的环境灾难呢?下面谈谈有关氰化物的知识。
一、氰化物的应用
氰化物是指氢氰酸(HCN)的盐类,它广泛用于电镀、冶金、合成医药等方面。
氰化物中碱金属氰化物易溶于水,水解呈碱性:
CN-+H2O=HCN+OH-
重金属氰化物难溶于水,但由于CN-的强配合作用,故而在碱金属氰化物中变得可溶了。所以,NaCN、KCN被用于从矿物中提取金和银。
乌鲁尔金矿是由澳大利亚一家金矿公司和罗马尼亚一家司合资开采。具体方法是:
先用NaCN或KCN的稀溶液处理粉碎的矿石,然后用Zn进行置换,使金从溶液中析出,有关反应可表示为:
4Au+8NaCN+2H2O+O2=4Na[Au(CN)2]+4NaOH
2Na[Au(CN)2]+Zn=2Au+Na2[Zn(CN)4]
提取金以后的氰化物废水流入废液池中等待进一步处理,而露天的氰化物废液池在大雨的连续浸袭后,漫池坝而过才酿成了这次欧洲环境大灾难。
氰化物的毒性
概述
氢氰酸和氰化物都有剧毒,而且中毒非常迅速。它们可以通过多种途径进入人体,如皮肤吸收、伤口侵入、呼吸道吸入、误食等,而水质和环境的污染使人和其他生物体被动吸收更是防不胜防。进入人体后,它能使中枢神经系统瘫痪,使呼吸酶及血液中血红蛋白中毒,引起呼吸困难,全身细胞会因缺氧窒息而使机体死亡。氰化物的中毒很少量就能使人致死,例如,氰化钠的致死量为0.05g。
欧洲环境大灾难中所有生物短时间内暴亡,仅死亡的鱼类就达100多万吨,由此可见氰化物毒性之一斑。
为保护我国人民的身心健康,环保部门制订了电镀、冶金、煤气等工业废水中CN-容许排放的最高浓度为0.0005g/L。
毒理作用
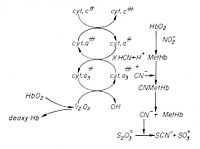
氰化物进入机体后分解出具有毒性的氰离子(CN-),氰离子能抑制组织细胞内42种酶的活性,如细胞色素氧化酶、过氧化物酶、脱羧酶、琥珀酸脱氢酶及乳酸脱氢酶等。其中,细胞色素氧化酶对氰化物最为敏感。氰离子能迅速与氧化型细胞色素氧化酶中的三价铁结合,阻止其还原成二价铁,使传递电子的氧化过程中断,组织细胞不能利用血液中的氧而造成内窒息。中枢神经系统对缺氧最敏感,故大脑首先受损,导致中枢性呼吸衰竭而死亡。此外,氰化物在消化道中释放出的氢氧离子具有腐蚀作用。吸入高浓度氰化氢或吞服大量氰化物者,可在2-3分钟内呼吸停止,呈“电击样”死亡。
氰化物废水及污染的处理
概述
由于氰化物有剧毒性,因此对于含氰化物的废水以及一旦造成氰化物的污染必须加以处理。
处理的方法主要是利用CN-的性质:
1.强配合性
工业上可加入FeSO4使之生成无毒物质,可表示为:
FeSO4+6NaCN=Na4[Fe(CN)6]+Na2SO4
2.还原性
CN-的还原性比I-弱,比Br-强,可被NaClO,Cl2等氧化剂所氧化,可表示为:
NaClO+NaCN=NaCNO+NaCl(NaCNO无毒)
5Cl2+10NaOH+2NaCN=2NaHCO3+N2↑+10NaCl+4H2O
欧洲这次环境大灾难,受污染的欧洲各国立即召开了紧急会议,沿河各大小城镇都成立了紧急指挥中心,制订了最大限度地减少被污染的河水造成的对环境的灾难性破坏的具体措施。
但是处理和补救只能减少污染所造成的危害,也是事后的一种无可奈何的选择,而已经造成的损失却难以弥补。环境专家说,这次欧洲环境灾难要想完全恢复这里的生态平衡,至少需要20年的时间。因此,更重要的是要通过这次环境灾难,警醒保护环境的重要性,提高世界人民以及我国人民的环境意识,保护好我们赖以生存的环境。
事实上,欧洲的这次环境灾难是罗马尼亚环保工作未受到应有的重视,政府至今未设环保基金,环保专业人员严重不足,公民环保意识淡薄。据消息说,这次金矿的氰化物泄漏并非因为雨水过大水位瀑涨而溢出,而是因为氰化物废液池的堤坝决口所致。金矿公司不承认是堤坝决口所致,只不过是想推卸部分责任。
性质:
由碳和氮两种原子组成一价原子团—C≡N或—CN。无机化合物中的氰化物(如氰化钠)以及有机化合物中的烃基腈(如丙烯腈)和氰基酸(如氰基乙酸)等分子中都含有这种原子团。
|
|||||||||||||||||||||||||||||||||||
| 关于“氰基”的留言: | |
|
目前暂无留言 | |
| 添加留言 | |