营养学/维生素D
| 医学电子书 >> 《临床营养学》 >> 维生素 >> 维生素D |
| 临床营养学 |
|
|
5.3.1 结构与性质
维生素D(VD)是环戊烷多氢菲类化合物,可由维生素D原(ProvitaminD)经紫外线270~300nm激活形成。动物皮下7-脱氢胆固醇,酵母细胞中的麦角固醇都是维生素D原,经紫外线激活分别转化为维生素D3及维生素D2量少,但人工照射者多为此型(图5-6)。维生素D的最大吸收峰为265nm,比较稳定,溶解于有机溶媒中,光与酸促进异构作用,应储存在氮气、无光与无酸的冷环境中,油溶液加抗氧化剂后稳定,水溶液由于有溶解的氧不稳定。双键系统还原也可损失其生物效用。
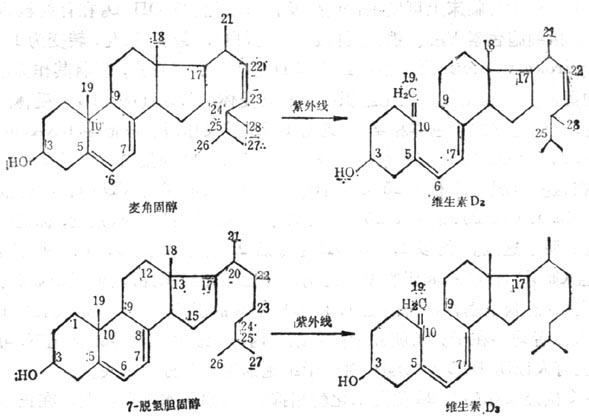
图5-6 麦解固醇及7-脱氢基胆固醇在紫外线作用下转变为维生素D2及维生素D3
5.3.2 代谢
从食物中得来的维生素D,与脂肪一起吸收,吸收部位主要在空肠与回肠。胆汁帮助其吸收。脂肪吸收受干扰时,如慢性胰腺炎、脂肪痢及胆道阻塞都会影响他的吸收。吸收的维生素D与乳糜微粒相结合,由淋巴系统运输,但也可与维生素D运输蛋白(α-球蛋白部分)相结合在血浆中运输。有些与β-脂蛋白相结合,口服维生素D与乳糜微粒结合,比从皮肤中来的与蛋白结合者易于分解。
当维生素D运到肝脏中,在微粒体中经单氧酶系统作用,将其25位羟基化形成25(OH)D(25-hydroxy vitamin D3)(图5-7),肝外的其他组织也可吸取维生素D及25-(OH)D3,因此组织中维生素D及25(OH)D3及其总量比血浆中多,如果靶组织需要,可将其释放出来,他们在脂肪组织中最多,释放速度最慢,当体重减轻,脂肪减少时,他们也可释放出来。静脉注射维生素D,较快的由血浆进入到组织中。血浆中25(OH)D3在注射后1~3天达到高峰,其浓度可达到20~40ng.ml-1,最高可达80ng.ml-1。浓度与摄入量有一定的关系,小于4 ng.ml-1,临床上可发生佝偻病及骨质软化。25(OH)D3在肾线粒体单氧酶作用下(酶系统包括细胞色素P450、铁硫蛋白及黄素蛋白),经羧基化,转变为1,25(OH)2D3(1,25-dihydroxy vxtamin D),他是维生素D的生物作用形式,现将其作为激素。其作用方式与其他固醇类激素相似。在靶组织中都有其受体,1,25(OH)2D3与受体形成复合物内,与细胞核或染色体相结合,通过DNA转录作用合成信使RNA(mRNA),并转译为蛋白质,1,25(OH)2D3在血浆中由分子量为52,00的蛋白质输送至靶组织(如小肠、骨、肾等),在这些组织中既有1,25(OH)2D3的受体,又有需要VD的钙结合蛋白(Calcium binding Protein,CaBP),说明1,25(OH)2D3的影响。最近,报道胰脏内有1,25(OH)2D3及CaBP,二者均存在于分泌胰岛素的β细胞内,在维生素D空竭情况下,可以阻止胰岛素的分泌,也有人证明1,25(OH)2D3对于干细胞的生长与分化有关。
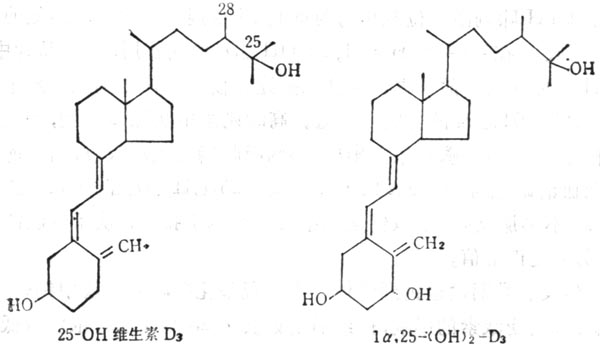
图5-7 25-(OH)D3及1a;25(OH)2D3的结构式
在肾中1位羧基化酶与24位羧基化酶相抑制,为血钙水平所控制。在正常血钙浓度下(9.5mg%)肾中1α羧基化酶与24位羧基化酶都有活力,所以既能合成1,25(OH)2D3也能合成24,25(OH)2D3,血清钙低时,刺激1位羧基化酶,钙多时抑制此酶。由此以调节1,25(OH)2D3合成之量。1,25(OH)2D3合成量多,24,25(OH)2D3合成量少,除血钙外,尚有其他因素影响1,25(OH)2D3如甲状旁腺素(Parthormone,PTH)、降钙素(Calcitonin,CT)、催乳激素都可使其增多。肾为2个羧基化的主要组织,但在体外试验已证明骨、胎盘、肠及蛋黄均有此功能。
1,25(OH)2D3的分解代谢与24,25(OH)2D3的途径相类似。24位羧基化后可进一步氧化成24位氧络物,然后23位羧基化,侧链分裂。26-C,27-C可氧化CO2水溶性代谢物有维生素D3-23羧酸(Calcitroic acid),也可产生内酯及酸酯,维生素D的分解代谢主要场所在肝内,并将其代谢物排入到胆汁中,口服维生素D比从皮肤中得来的易于分解。25(OH)2D3及1,25(OH)2D3也可以葡糖苷酸形式通过胆肝形成肝肠循环或从大便中排出。口服生理剂量48h后,30%的剂量从大便中排出,仅2-~4%从尿中排出。
5.3.3 生理功用
(1)维持血清钙磷浓度的稳定 血钙浓度低时,诱导甲状旁腺素分泌,将其释放至肾及骨细胞。在肾中PTH除刺激1位羧化酶与抑制24位羧基化酶外,还促使磷从尿中排出,钙在肾小管中再吸收。在骨中PTH与1,25(OH)2D3协同作用,将钙从骨中动员出来。在小肠中1,25(OH)2D3促进钙的吸收。从这三条途径使血钙恢复到正常水平,又反馈控制PTH的分泌及1,25(OH)2D3的合成。在血钙高时刺激甲状腺C细胞,产生降钙素,阻止钙从骨中动员出来,并促使钙及磷从尿中排出。小肠吸收磷为主动吸收,需要能量,钠、葡萄糖、1,25(OH)2D3及血清磷低时(8mg%以下),刺激1,25(OH)2D3的合成,促进小肠对钙、磷的吸收。由于PTH不参加反应,所以钙从尿中排出而磷不排出,从而使血钙略有上升,而磷上升较多,使血磷恢复正常值。
(2)促进怀孕及哺乳期输送钙到子体 1位羧基化酶除受血清中钙磷浓度及膳食中钙磷供给量的影响外,还受激 素的影响,停经后的妇女1,25(OH)2D3浓度减低,易有骨质软化等症状。
在怀孕期间1,25(OH)2D3血浆浓度上升,哺乳期继续上升,断乳后母体逐渐恢复到正常水平。24,25(OH)2D3之水平与之相反,怀孕期下降,断乳后恢复到正常。胎盘也有1位羧基化酶,在怀孕期间无肾动物也能合成1,25(OH)2D3。乳腺也是1,25(OH)2D3的靶组织,对乳中钙的水平直接关系,怀孕及哺乳期间母亲可从自身的骨中将钙输出以维持胎儿婴儿正常生长,维生素D供应充足者,在断乳后,又可重新获得钙,维生素D缺乏者,这种恢复能力较差。
(3)1,25(OH)2D3作用机理 1,25(OH)2D3对小肠作用为诱导合成CaBP.1,25(OH)2D3与小肠细胞的受体形成复合体进入细胞核染色体上,促使CaBP的信使RNA(mRNA)的合成,此mRNA在胞浆内转录为CaBP。这种蛋白促使钙离子通过微绒毛刷状缘(microvillus brush border),积累于肠细胞的线粒体或其他部位。通过Na+将Ca2+挤出基底-外侧膜外(basal-lataaral mebrace)。1,25(OH)2D3对肾小管Ca2+的再吸收作用与在小肠中是一样的。1,25(OH)2D3也可以在低血浆钙及膳食中钙缺乏时,将钙从骨中动员出来,但在骨中未发现有CaBP,1,24,25(OH)2D3可以促进小肠吸收钙,但不能从骨中将钙动员出来,所以1,25(OH)2D3对骨的作用机理与对小肠者是不同的,但目前还不清楚。
骨的矿物化作用的机理尚未阐明,补充1,25(OH)2D3给缺乏维生素D的动物及人体,都不能有助于骨中矿物质的沉积。动物体内虽然分离出许多维生素D代谢产物但迄今尚未找出对骨的矿物化有明显作用者。在现阶段中只了解到维生素D促进钙磷的吸收,又可将钙磷从骨中动员出来,使血浆钙、磷达到正常值,促使骨的矿物化,并不断更新。
5.4.3 需要量
(1)维生素D的营养指标血清中碱性磷酸酶增加比维生素D缺乏的临床症状出现要早一些,他的增加幅度也与维生素D缺乏的程序有关,但是他是非特异性的(表5-7)。血清中Ca与P的乘积(mg%),正常值为36~40。佝偻病及骨质软化患者的乘积在30以下。
表5-7 正常人及病人血清碱性磷酸酶、钙、磷浓度
| 血清碱性磷酸酶(布氏单位.ml-1 (国际单位umol.mm-1.L-1) | 血清Ca(mg%) | 血清P(mg%) | ||
| 正常婴儿 | 5~15 | 26~80 | 10 | 5 ~ 8 |
| 正常成人 | 3~5 | 16~26 | 10 | 3~4.5 |
| 佝偻病人 | >20 | >115 | 8~9 | 3 |
| 骨质软化病人 | 15 | 80 | 9 | 2~3 |
| 甲状旁腺素过多 | 4~20 | 20~120 | 12~16 | 2~8 |
| 骨质疏松 | 2 | 10 | 10~12 | 4~5 |
| 变形性骨炎(Paget's) | 50 | 268 | 10 | 4 |
| 成骨细胞瘤 | 30 | 160 | 10 | 4 |
静脉注射1mg维生素D后,测定其血清磷值,隔5天后再测定饥饿时血清磷值,若其值增加,则可为维生素D缺乏的指标。口服磷酸钠盐24h后,血浆Ca值减低。腕部骨骺部增大也是一个简单诊断佝偻病的方法。
现在用同位素蛋白结合方法测定25-(OH)D3,或1,25(OH)D3,正常人血中25-(OH)D3浓度为15.2±5.6ng.ml-1,若小于4ng.ml-1,临床上易有佝偻病及骨质软化。1,25(OH)D3血浆正常。水平为3~6ng.ml-1,但由于这方面工作不多,其正常低限与最理想水平尚未确定。
(2)维生素D需要量由于日光照射皮肤可产生维生素D,从外界应予补充量受日光照射的影响,宇身航员未得到日光照射1~3个月久,每天给以维生素D或25(OH)D310ug可以维持血浆25(OH)D3的正常水平。从出生到青春期供应量为10ug(400IU)孕妇乳母10ug。在整个生命过程中,钙磷进行动态平衡,骨骼不断进行重建,成人也需要一定量的维生素D约为5ug。
5.3.5 来源
鱼肝油、牛奶、蛋黄等动物性食品中有维生素D3,蕈及麦角中维生素D2,皮肤中7-脱氢胆固醇经紫外线照射变为维生素D3前体(Previtamin D3),然后在一定温度下异构为维生素D3,这一过程比较缓慢,37℃时维生素D3可达80%,温度低时转换率小些。皮肤中维生素D3与前体仍继续异构为维生素D3为机体所利用。因其转变过程缓慢,不致产生毒性,血浆25(OH)维生素D3不超过80%,温度低时转换率小些。皮肤中维生素D3与前体呈一定的平衡。血浆中有维生素D3结合蛋白,可将维生素D3从皮肤中带到血流中,这种蛋白不与前体结合。为了获得新的平衡,前体不断地变成维生素D3。停止照射后,皮肤中储存的前体仍继续异构为维生素D3为机体所利用。因其转变过程缓慢,不致产生毒性,血浆25(OH)维生素D3不超过80ng.ml-1,摄取大剂量者可上升到400 ng.ml-1,易产生毒性。
5.3.6 临床应用及大剂量的毒性
维生素D除防治维生素D3缺乏病外1,25(OH)2D3可防治下列病症:①肾性骨病,肾功能不全缺少1位羟基化酶,体内不能合成1,25(OH)2D3必须从体外摄取;②难治疗抗维生素D3佝偻病,由于遗传因素,磷从肾排出过多;③甲状旁腺素缺少症,患者不能在低血浆Ca时产生1,25(OH)2D3;④抗维生素D的佝偻病,维生素D供应正常但仍有佝偻病,由于代谢上的缺陷,不能1位羧基化;⑤癫痫病人使用苯巴比妥可能导致骨病。也可用25(OH)2D3的生理剂量为1μg/天。此剂量也可作为治疗剂量。
维生素D中毒剂量与生理剂量相差不多,婴儿服用50μg(200IU)或更少一些可以导致血钙过多,肾功能不全。成人中毒剂量个体差异较大,有人口服2000IU中毒现象,口服5000IU者易中毒,口服量不能超过800IU。用维生素D治疗时,要检查血钙水平,如血钙正常不致中毒,轻度中毒有呕吐,食欲不振等现象,重者可致死亡。维生素D毒性可由于血流中25(OH)2D3水平高代替1,25(OH)2D3与蛋白受体结合,因此1,25(OH)2D3不能进入细胞,也不能起控制钙的吸收及动员骨钙的作用,因此血钙水平高,而使肾、心脏及主动脉钙化,治疗维生素D过多时可用低钙膳及动员骨钙的作用,因此血钙水平高,而使肾、心脏及主动脉钙化,治疗维生素D过多时可用低钙膳及糖皮质激素以减低血清钙的水平。
中毒时尿中排出Ca量过多比血钙过高发生较早,尿钙过高易形成肾结石。
维生素D及25(OH)D3可以储存,维生素D储存时间一般为1~4个月,有的可达18个月久。维生素D代谢物也可产生中毒现象,但由于其生物半衰期短,中毒时间也较短,25(OH)D3可达数周,1,25(OH)2OH3仅有数日。
参看
| 关于“营养学/维生素D”的留言: | |
|
目前暂无留言 | |
| 添加留言 | |