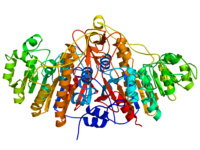
碱性磷酸酶
| A+医学百科 >> 碱性磷酸酶 |
目录 |
生物化学特征
碱性磷酸酶名字
alkaline phosphatase (ALP 或 AKP)
现多用ALP
系统名phosphate-monoester phosphohydrolase (alkaline optimum)
其他名称还有alkaline phosphomonoesterase; phosphomonoesterase; glycerophosphatase; alkaline phosphohydrolase; alkaline phenyl phosphatase; orthophosphoric-monoester phosphohydrolase (alkaline optimum);basic phosphatase
CAS 号: 9001-78-9
碱性磷酸酶
属于同源二聚体蛋白,分子量为56KDa。每个单体由449个氨基酸组成,完整的AKP分子呈现典型的α/β的拓扑结构,同时每个单体均具有一个活性中心,活性中心区域由Asp101-Ser102-Ala103三连体、Arg166、水分子、三个金属离子及其配体氨基酸组成。AKP被phoA 基因编码,与很多分泌蛋白一样,在细胞质内合成氨基末端带有信号肽的单体前体,信号肽引导前体跨内膜运输后被切除,同源二聚体形成。
碱性磷酸酶是一种能够将对应底物去磷酸化的酶,即通过水解磷酸单酯将底物分子上的磷酸基团除去,并生成磷酸根离子和自由的羟基,这类底物包括核酸、蛋白、生物碱等。而该脱去磷酸基团的过程被称为去磷酸化或脱磷酸化。碱性磷酸酶是磷酸酶的一种,磷酸酶的作用与激酶的作用正相反,激酶是磷酸化酶,可以利用能量分子,如ATP,将磷酸基团加到对应底物分子上。碱性磷酸酶在碱性环境有最大活力,对来源于细菌中的ALP来说,其最适pH是8.0,而对来源于牛的ALP则是8.5。
ALP是一种含锌的糖蛋白,在碱性环境中(最适Ph为10左右)可以水解各种天然及人工合成的磷酸单酯化合物底物。
人体内的来源
人体内情况
碱性磷酸酶是广泛分布于人体各脏器器官中,其中以肝脏为最多其次为肾脏,骨骼、肠、和胎盘等组织,。这种酶能催化核酸分子脱掉5’磷酸基团,从而使DNA或RNA片段的5’-P末端转换成5’-OH末端。但它不是单一的酶,而是一组同功酶。目前已发现有 AKP1 、 AKP2 、 AKP3 、 AKP4 、 AKP5 与 AKP6 六种同功酶。其中第 1 、 2 、 6 种均来自肝脏,第 3 种来自骨细胞,第 4 种产生于胎盘及癌细胞,而第 5 种则来自小肠绒毛上皮与成纤维细胞。 血清中的ALP主要来自肝脏和骨骼。生长期儿童血清内的大多数来自成骨细胞和生长中的骨软骨细胞,少量来自肝。尿中的直接来自于肾小管细胞,并非来源于血液。
碱性磷酸酶主要用于阻塞性黄疸、原发性肝癌、继发性肝癌、胆汁淤积性肝炎等的检查。患这些疾病时,肝细胞过度制造ALP,经淋巴道和肝窦进入血液,同时由于肝内胆道胆汁排泄障碍,反流入血而引起血清碱性磷酸酶明显升高。但由于骨组织中此酶亦很活跃。因此,孕妇、骨折愈合期、骨软化症。佝偻病、骨细胞癌、骨质疏松、肝脓肿、肝结核、肝硬变、白血病、甲状腺机能亢进时,血清碱性磷酸酶亦可升高,应加以鉴别。
研究应用
碱性磷酸酶也是目前免疫诊断试剂产品最常用的标记酶之一。与辣根过氧化物酶(HRP)相比,ALP用作标记酶的优点是,稳定性高、灵敏度高,缺点是成本高,标记困难。
在研究中最常用的ALP如下:
◇细菌碱性磷酸酶Bacterial alkaline phosphatase (BAP), 来源:Escherichia coli C4 ;
◇ Shrimp alkaline phosphatase (SAP), 来源:一种北极虾 (Pandalus borealis) ;
◇ 小牛肠碱性磷酸酶Calf Intestinal Alkaline Phosphatase (CIP);
◇ 胎盘碱性磷酸酶Placental alkaline phosphatase (PALP)和分泌性碱性磷酸酶the secreted alkaline phosphatase (SEAP),后者是前者的C末端短缺版——与PALP相比,SEAP没有PALP的C末端最后24个氨基酸(这24个氨基酸构成了与糖基化磷脂酰肌醇靶向锚定的区域)
ALP主要应用于分子生物学和酶免分析中:
★分子生物学中主要用作核酸的去磷酸化。因为DNA通常会在5'端结合磷酸基团,用ALP去磷酸化能防止DNA分子5'端与3'端连接,从而在后续步骤准备好之前让DNA分子抑制处于线性化状态;同样,通过去磷酸化可用作放射标记示踪。通常用作这些目的用的最多的是Shrimp alkaline phosphatase (SAP),因为在反应完成之后它是最容易灭活的。
★酶免分析中应用最多的是ELISA,以竞争法测小分子抗原为例,抗体先与固相载体结合,然后让待测样品与事先经ALP标记过的该抗原竞争地与抗体结合,洗去未反应的过量ALP-抗原,加入显色底物。则可以通过与按梯度浓度变化的标准品绘出的标准曲线对比从而知道待测样品中抗原的浓度。ELISA中用的比较多的是 辣根过氧化物酶(HRP),底物为OPD, 深桔黄色 ,检测波长492nm;TMB, 蓝绿色,检测波长450nm 碱性磷酸酶,底物为PNPP(对-消基苯磷酸酯), 黄色 ,检测波长405nm
★目前工业上一个普遍的应用是作为检验牛奶的巴斯的灭菌的标志:被巴斯德过高温灭菌的分子会被灭活,向其中和未巴斯灭菌的牛奶中加入ALP的底物,2分钟后未灭菌的样品应该显黄色,如果待测样品(指被巴斯灭菌过的牛奶)也能呈现相同颜色,则说明巴斯灭菌温度未过度。当然总有例外,因为有少数细菌会产生耐热的ALP。
测定方法
有很多种,我国曾应用较广的为磷酸苯二钠比色法,但现在应用较多的是连续检测法。
正常范围
正常范围(连续监测法)
女性,1-12岁小于500U/L;大于15岁,40-150U/L;
男性,1-12岁小于500U/L;12-15岁,小于750U/L;大于15岁,40-150U/L。
高值可能说明有单管阻塞现象;低值更多出现于儿童和孕妇身上。高值表明有可能发生了活性骨沉积(这个可能译的不准,请指正,原文为active bone deposition),因为ALP是成骨细胞活动(造骨)的副产物(例如在佩吉氏斯症[畸形性骨炎]的案例中)。
一般来说,低值要比高值少见。
临床意义
临床上测定ALP主要用于骨骼 、肝胆系统疾病的诊断和鉴别诊断,尤其是黄疸的鉴别诊断。对于不明原因的高ALP血清水平,可测定同工酶以协助明确其器官来源。
1.生理性增高:儿童在生理性的骨骼发育期,碱性磷酸酶活力可比正常人高1~2倍。处于生长期的青少年,以及孕妇和进食脂肪含量高的食物后均可以升高。
2.病理性升高:
(1)骨骼疾病如佝偻病、软骨病、骨恶性肿瘤、恶性肿瘤骨转移等;
(2)肝胆疾病如肝外胆道阻塞、肝癌、肝硬化、毛细胆管性肝炎等;
(3)其他疾病如甲状旁腺机能亢进。
3.病理性降低:见于重症慢性肾炎、儿童甲状腺机能不全、贫血等。
抑制作用
除来源于胎盘外所有哺乳动物的ALP同工酶都能被高精氨酸所抑制;而除来源于肠和胎盘外所有的ALP同工酶都能被左旋咪唑所抑制;而除了来源于胎盘的ALP(PALP和SEAP)外,几乎所有的ALP都能在65℃2小时即被灭活。
单乙醇胺对碱性磷酸酶有温度依赖的抑制作用;
较高浓度的无机磷可竞争性地抑制碱性磷酸酶的活性;
EDTA通过络合碱性磷酸酶而导致该酶活性中心微环境构象发生变化,从而不可逆地抑制碱性磷酸酶的活性;
其他的抑制剂还有联苯胺(竞争性)、L-苯丙氨酸和丹酰-L-苯丙氨酸(反竞争性)、含氮杂环氧钒配合物(选择性)、五氯酚(对人胎盘碱性磷酸酶反竞争性抑制)等。
| 关于“碱性磷酸酶”的留言: | |
|
目前暂无留言 | |
| 添加留言 | |