医学影像学/经皮血管腔内血管成形术
| 医学电子书 >> 《医学影像学》 >> 介入放射学 >> 血管介入技术 >> 经皮血管腔内血管成形术 |
| 医学影像学 |
|
|
经皮血管腔内血管成形术(percutaneoustransluminal angioplasty,PTA)是经导管等器械扩张再通动脉粥样硬化或其他原因所致的血管狭窄或闭塞性病变,这一疗法是60年代开始应用的,在80年代前主要采用球囊导管进行治疗,称为球囊血管成形术(balloon angioplasty)。在80年代陆续出现了几种血管成形术的新技术,主要是激光血管成形术(laser angioplasty)。粥样斑切除术(atherectomy)、血管内支撑器(endovascular stent)等。
PTA原来主要用于肢体血管,以后扩展至内动脉,如肾动脉、冠状动脉,并且由动脉发展至静脉,如扩张治疗腔静脉狭窄,以至治疗人造血管、移植血管的狭窄或闭塞。
一、球囊血管成形术
(一)适应证 理想的适应证是中等大小或大血管局限、孤立性短段狭窄。其次为多发、分散的短段狭窄和闭塞。长段狭窄或闭塞、小血管病变、溃疡性狭窄或已有钙化的狭窄或闭塞病变不适宜于PTA治疗。
(二)操作技术 在血管造影确定病变位、程度和侧支供血情况以及狭窄上下方的血压等血液动力学改变后,将造影导管调换成球囊导管(图6-1-3)。将球囊置于狭窄区,用压力泵或手推稀释的造影剂充胀球囊。充胀的球囊作用于狭窄的血管,使之发生扩张。扩张结束后,要复查血管造影,了解血管扩张情况,同时再次测量原狭窄区上下方的血压差以确定扩张治疗的效果。为了减少并发症和预防再狭窄,从术前一天开始应用抗血小板聚集药物,如阿司匹林等。术中要用肝素抗凝,术后1~6个月服用阿司匹林、潘生丁等药物。
(三)血管扩张的机理 充胀的球囊压力造成了狭窄区血管壁内、中膜局限性撕裂。血管壁特别是中膜过度伸展以及动脉粥样斑的断裂,从而导致血管壁张力减退和腔径的扩大。
(四)疗效 PTA的近期和远期疗效均较好。髂、肾动脉的PTA成功率在90%以上,五年均血管开放率在70%以上。冠状动脉脉单支病变PTA成功率在90%以上。影响疗效的因素中,除病变部位外,病变性质、病变的解剖与病理学特征、患者全身状况、设备情况以及术者经验等也是重要因素。例如在肾动脉狭窄中,以纤维肌发育不良的疗效最好,扩张成功率在90%~95%,临床上高血压治愈和改善率达93%;其次为动脉粥样硬化症;而多发性大动脉炎的疗效较差。
PTA比外科手术的优点在于对患者创伤小,并发症少,收效快,操作较简便,减少用费,门诊即可进行,一旦发生再狭窄可以重复PTA治疗。
(五)再狭窄问题 PTA虽然具有较好的疗效,但是扩张后再狭窄的发生率较高,平均发生率约为30%。再狭窄多发生在PTA后数月至1年内。主要原因是球囊扩张部位内膜纤维细胞增生的结果。扩张的机理表明,成形术是一种损伤血管壁成分的机械治疗方法,术后必然会引起一系列修复反应,这就成为再狭窄的病理学基础.因此球囊扩张的结局具有两重性。内、中膜局限性撕裂造成了血管腔的扩大,血流灌注得以恢复;同时内、中膜撕裂也成为纤维组织增生导致再狭窄的原因。
再狭窄的其他原因是血管壁的弹性回缩和原有病变的进展。
为了减少再狭窄,可采取以下三种措施:①改进设备:已研制成新型成新型材料的球囊,可减少对血管的损伤。②药物治疗:减少、预防和治疗PTA进程中和PTA后出现的血管痉挛、血小板粘附、血栓形成和内膜纤维细胞增生。常用药物为阿司匹林、肝素、硝苯吡啶(心痛定)硝酸甘油以及正在试用的前列腺环素、血栓素合成酶抑制剂等。③新技术的应用:即下述几项血管成形术。
(六)并发症 PTA的并发症较少,有时可发生穿剌局部血肿、动脉壁撕裂孔、远侧端血管塞以及球囊破裂等。
二、激光血管成形术
80年代初用于再通外周动脉,现已大量用于临床,取得了很有希望的疗效,激光能量消融粥样斑或血栓使血管再通的机理,主要在于热效应和化学解吸作用。
激光源有气体、固体和液体等物质。激光血管成形术用得较多的是钕钇铝石榴石(Nd-YAG)激光和准分子(excimer)激光。传输系统用多根石英纤维。为减少血管发生穿孔,在石英端头加用金属帽、蓝宝石帽。激光以连续或脉冲方式发射。连续发射可造成组织的明显热损伤。脉冲发射能量多,易消融病变组织,也无明显的热损伤。故现多用脉冲波。激光波长可采用紫外线(200~400mm)。可见光(400~700mm)或红外线(700~1000nm)。
激光血管成形术可能有以下优点:①治疗血管慢性闭塞、弥漫病变、钙化病变优于球囊血管成形术,而且对球囊成形术后出现的急性血管闭合有效。②热效应热抛光或封焊作用,在球囊扩张后接着应用,可使球囊扩张所造成的血管腔面由不规则变平滑,且封焊剥离的内膜,从而减少血小板粘附近和血栓形成。③光热作用可改变血管壁的顺应性,降低动脉壁对血管活性物质的反应,减轻球囊扩张后所引起的血管壁弹性回缩,有利于血管的持久扩张。因此,激光血管成形术现多与球囊血管成形术配合应用,称之为激光辅助球囊血管成形术(laser-assisted balloon angioplasty)。
激光再通血管仍处于研究开发阶段,有许多技术问题需进一步解决。
三、动脉粥样斑切除术
有些学者简称之为旋切法,主要适用于血管高度狭窄或完全闭塞,也是一种机械治疗方法。
按照用于这一疗法的导管功能看,其治疗方式分为两种:①经皮切割,取出粥样物质,称之为atherectomy,意即切除术:②经皮破碎粥样斑,使之成为微粒,存留于血液循环中,有待于机体自然清除,称之为atheroablation,意即破碎术。
用于这一治疗的导管头端有一高速或低速旋转的削刀或磨球,当导管头端置于血管闭塞病变处,操纵体外导管尾端驱动装置,削刀或磨球旋转,切除或磨碎病变,使血管再通。正在研制的导管很多,目前用于临床的有Kensey导管、Simpson导管、经腔抽吸导管(TEC)等。
旋切法除用于外周血管外,也开始用于肾动脉和冠状动脉。外周血管的再通成功率在95%以上。由于旋切法仍是机械性治疗手段,所以损伤血管壁后的修复反应还可造成再狭窄。这一疗法也在发展中。
四、血管支撑器
血管支撑器是采用特殊的合金,制成不同结构的圆筒形,支撑于血管狭窄病变处,使之保持血流通畅。目前支撑器有三种:①热记忆合金支撑器(thermal memory alloy stent):由镍钛合金丝制成,称为Nitinol。②自膨支撑器(self-expandablestent);用不锈钢合金丝编织成圆筒形,放入血管后,由于金属弹力而支撑于血管腔内。③球囊膨支撑器(balloon-expandable stent):支撑器是圆筒网眼形,先在球囊之上,放入血管后充胀球囊,使支撑器张开支撑于血管腔内(图6-1-4)。
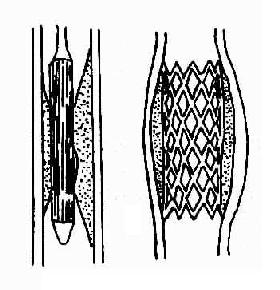
图6-1-4 球囊膨胀支撑器
支撑器置与血管后,机体能耐受,无异物反应。支撑器内表现由于纤维蛋白原覆盖,不久即可形成新生内膜,同支撑器两端处的正常血管内膜相接,从而保证血管的通畅。
支撑器主要同球囊血管成形术、激光血管成形术和旋切法等相配合应用。在后几种技术扩张或再通病变血管后。放置支撑器,可提高血管开放率,减少再狭窄。
此外,利用超声能量消除粥样斑、血栓等以再通血管也试用于临床,称之为超声血管成形术(ultrasonic angioplasty ,angiosonoplasty)。一些新的血管影像技术,如血管镜、血管内超声和MRA对于经皮血管成形术的发展有重要作用。
参看
| 关于“医学影像学/经皮血管腔内血管成形术”的留言: | |
|
目前暂无留言 | |
| 添加留言 | |