生理学/神经-骨骼肌接头处的兴奋传递
| 医学电子书 >> 《生理学》 >> 细胞的基本功能 >> 肌细胞的收缩功能 >> 神经-骨骼肌接头处的兴奋传递 |
| 生理学 |
|
|
|
运动神经纤维在到达神经末梢处时先失去髓鞘,以裸露的轴突末梢嵌入到肌细胞膜上称作终板的膜凹陷中,但轴突末梢的膜和终板膜并不直接接触,而是被充满了细胞外液的接头间隙隔开,其中尚含有成分不明的基质;有时神经末梢下方的终板膜还有规则地再向细胞内凹入,形成许多皱褶,其意义可能在于增加接头后膜的面积,使它可以容纳较多数目的蛋白质分子,它们最初被称为N-型乙酰胆碱受体,现已证明它们是一些化学门控通道,具有能与ACh特异性结合的亚单位。在轴突末梢的轴浆中,除了有许多线粒体外还含有大量直径约50nm的无特殊构造的囊泡(图2-19)。用组织化学的方法可以证明,囊泡内含有ACh;此ACh首先在轴浆中合成,然后贮存在囊泡内。据测定,每个囊泡中贮存的ACh量通常是相当恒定的,且当它们被释放时,也是通过出胞作用,以囊泡为单位“倾囊”释放,被称为量子式释放。在神经末梢处于安静状态时,一般只有少数囊泡随机地进行释放,不能对肌细胞产生显著影响。但当神经末梢处有神经冲动传来时,在动作电位造成的局部膜去极化的影响下,大量囊泡向轴突膜的内侧面靠近,通过囊泡膜与轴突膜的融合,并在融合处出现裂口,使囊泡中的ACh全部进入接头间隙。据推算,一次动作电位的到达,能使大约200~300个囊泡的内容排放,使近107个ACh分子被释放。轴突末梢处的电位变化引起囊泡排放的过程十分复杂,但首先是轴突末梢膜的去极化,引起了该处特有的电压门控式Ca2+通道开放,引起细胞间隙液中的Ca2+进入轴突末梢,触发了囊泡移动以至排放的过程。Ca2+的进入量似乎决定着囊泡释放的数目;细胞外液中低Ca2+或(和)高Mg2+,都可阻碍ACh的释放而影响神经-肌接头的正常功能。已故冯德培院士在30年代对神经-肌接头的化学性质传递进行过重要的研究。
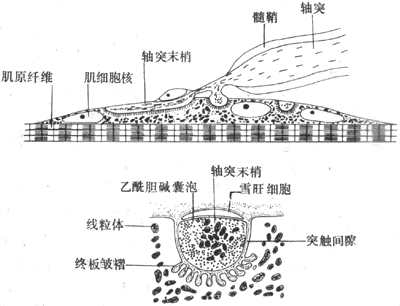
图2-19 神经-肌接头处的超微结构示意图
当ACh分子通过接头间隙到达终板膜表面时,立即同集中存在于该处的特殊通道蛋白质的两个α-亚单位结合,每分子的通道将结合两个分子的ACh,由此引起的蛋白质分子内部构象的变化会导致它的通道结构的开放。这种通道开放时,孔道的横截面比前面提到的Na+通道的面积为大,可允许Na+、K+甚至少量Ca2+同时通过;由于这几种离子正常时在膜内处的分布特点,实际出现的是Na+的内流和K+的外流,其总的结果是使终板膜处原有静息电位减小,向零值靠近,亦即出现膜的去极化;这一电变化,称为终板电位,它的出现约较神经冲动到达接头前膜处晚0.5~1.0ms。有人曾在运动神经无冲动到达末梢时,记录到由于个别囊泡的自发释放在终板膜上引起的微小的电变化,称为微终板电位。终板电位与前述的局部兴奋电反应有类似的性质:不表现“全或无”特性,其大小与接头前膜释放的ACh的量成比例;无不应期,可表现总和现象等,如我们一般记录到的终板电位就是多数微终板电位总和的结果。终板电位产生时,它将以电紧张性扩布的形式影响终板膜周围一般肌细胞膜。一般的肌细胞膜与神经轴突的膜性质类似,其中主要含电压门控式Na+通道和K+通道;因而当同终板膜邻接的肌细胞膜的静息电位由于终板电位的影响而去极化到该处膜的阈电位水平时,就会引发一次向整个肌细胞膜作“全或无”式传导的动作电位,后者再通过所谓“兴奋-收缩耦联”,引起肌细胞出现一次机械收缩。
正常情况下,一次神经冲动所释放的ACh以及它所引起的终板电位的大小,大约超过引起肌细胞膜动作电位所需阈值的3~4倍,因此神经肌接头处的兴奋传递通常是1对1的,亦即运动纤维每有一次神经冲动到达末梢,都能“可靠地”使肌细胞兴奋一次,诱发一次收缩;这一点与将来要讲的神经元之间的兴奋传递有明显不同(见第十章)。接头传递能保持1对1的关系,还要靠每一次神经冲动所释放的ACh能够在它引起一次肌肉兴奋后被迅速清除,否则它将持续作用于终板而使终板膜持续去极化,并影响下次到来的神经冲动的效应。已知,ACh的清除主要靠胆硷酯酶的降解作用来完成,此酶主要分布在接头间隙中和接头后膜上,它们大约可以在2.0ms的时间内将一次神经冲动所释放的ACh清除掉。许多药物可以作用于接头传递过程中的不同阶段,影响正常的接头功能。例如,美洲箭毒和α-银环蛇毒可以同ACh竞争终板膜的ACh受体亚单位,因而可以阻断接头传递而使肌肉失去收缩能力;有类似作用的药物称为肌肉松弛剂;有机磷农药和新斯的明对胆碱酯酶有选择性的抑制作用,可造成ACh在接头和其他部位的大量积聚,引起种种中毒症状。重症肌无力是由于体内骨骼肌终板处的ACh门控通道数量不足或功能障碍所引起。
| 关于“生理学/神经-骨骼肌接头处的兴奋传递”的留言: | |
|
目前暂无留言 | |
| 添加留言 | |