生理学/电压门控通道
| 医学电子书 >> 《生理学》 >> 细胞的基本功能 >> 细胞的跨膜信号传递功能 >> 由具有特异感受结构的通道蛋白质完成的跨膜信号传递 >> 电压门控通道 |
| 生理学 |
|
|
应用类似的技术,在80年代还陆续克隆出几种重要离子(如Na+、K+和Ca2+等离子)的电压门控通道,它们具有同化学门控能道类似的分子结构,但控制这类通道开放与否的因素,是这些通道所在膜两侧的跨膜电位的改变;也就是说,在这种通道的分子结构中,存在一些对跨膜电位的改变敏感的基团或亚单位,由后者诱发整个信道分子功能状态的改变。
在动物界,除了一些特殊的鱼类,一般没有专门感受外界电刺激或电场改变的器官或感受细胞,但在体内有很多细胞,如神经细胞和各种肌细胞,在它们的细胞膜中却具有多种电压门控通道蛋白质,它们可由于同一细胞相邻的膜两侧出现的电位改变而再现通道的开放,并由于随之出现的跨膜离子流而出现这些通道所在膜的特有的跨膜电位改变。例如,前述的终板膜由Ach门控通道开放而出现终板电位时,这个电位改变可使相邻的肌细胞膜中存在的电压门控式Na+通道和K+通道相继激活(即通道开放),出现肌细胞的所谓动作电位;当动作电位在神经纤维膜和肌细胞膜上传导时,也是由于一些电压门控通道被邻近已兴奋的膜的电变化所激活,结果使这些通道所在的膜也相继出现特有的电变化。由此可见,电压门控通道所起的功能,也是一种跨膜信号转换,只不过它们接受的外来刺激信号是电位变化,经过电压门控通道的开闭,再引起细胞膜出现新的电变化或其他细胞内功能变化,后者在Ca2+通道打开引起膜外Ca2+内流时甚为多见。
根据对Na+、K+、Ca2+三种离子的电压门控通道蛋白质进行的分子结构分析,发现它们一级结构中的氨基酸排列有相当大的同源性,说明它们属于同一蛋白质家族,与之有关的mRNA在进化上由同一个远祖基因演化而来。图2-8是与体内动作电位(见后)产生至关重要的Na+通道在膜内结构的模式图,它主要由一个较大的α-亚单位组成,分子量约260kd;有时还另有一个或两个小分子量的亚单位,分别称为β1和β2。但Na+通道的主要功能看来只靠α-亚单位即可完成。这个较长的α-单位肽链中包含了4个结构类似的结构域(domain,每个结构域大致相当于上述Ach门控通道中的一个亚单位,但结构域之间由肽链相连,是一个完整的肽链,应由一个mRNA编码和合成),而每个结构域中又各有6个由疏水性氨基酸组成的跨膜α-螺旋段(图示2-8,A);这4 个结构域及其所包含的疏水α-螺旋,在膜中包绕成一个通道样结构(图2-8,B)。现已证明,每个结构域中的第4个跨膜α-螺旋在氨基酸序列上有特点,即每隔两个疏水性氨基酸,就再现一个带正电荷的精氨酸或赖氨酸;这些α-螺旋由于自身的带电性质,在它们所在膜的跨膜电位有改变时会产生位移,因而被认为是该通道结构中感受外来信号的特异结构,由此再诱发通道“闸门”的开放;还有实验提示,每个结构域中的第2、第3个α-螺旋构成了该通道水相孔道的“内壁”;据测算,水相孔道内径最窄处横断面积约为0.3×0.5nm差不多刚能通过一个水化的Na+(图2-8,B)。
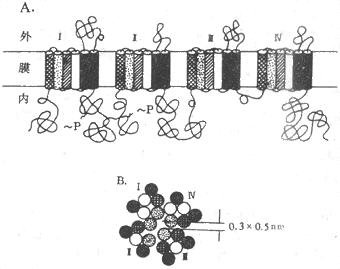
图2-8 电压门控Na+通道的分子结构示意图
A:构成电压门控Na+通道的α-亚单中的4个结构以及每个结构域中6个
B:4个结构域及其α-螺旋形成通道时的相对位置
参看
| 关于“生理学/电压门控通道”的留言: | |
|
目前暂无留言 | |
| 添加留言 | |