临床生物化学/光谱分析的常用方法
| 医学电子书 >> 《临床生物化学》 >> 常用分析技术在临床生物化学中的应用 >> 光谱分析技术的应用 >> 光谱分析的常用方法 |
| 临床生物化学 |
|
|
|
(一)吸收光谱分析法
1、可见光及紫外光分光亮度法
(1)标准曲线法:将一系列浓度不同的标准溶液按照一定操作过程显色后,分别测吸亮度,以吸亮度为纵坐标,浓度为横坐标绘制标准曲线。在相同条件下处理待测物质并测定其吸亮度,即可从标准曲线找出相对应的浓度。
(2)对比法:将标准样品与待测样品在相同条件下显色并测定各自的吸亮度。由于测定体系温度、厚度以及入射光波长是一致的,所以标准与待测样品K值及L相等,可应用下式比较计算待测样品浓度:Cx=Cs×As/Ax。
(3)差示法:有色溶液浓度太浓或太稀(透光度超过90%-10%)时,测定结果会产生较大误差,此时可采用差示法(differentialspectrophotometry)。①高浓度样液差示法:用标准品制备浓度稍低于试样的参比溶液,先将仪器光门关闭,调节T%=0,再将参比溶液置于光路上,打开光门使T%=100,然后测定样品溶液的透光率即可。例如某一样品溶液原来的透光率读数为5%(10%以下),用差示法后读数为50%,这实质是把透光率标尺扩展了10倍,从而减少了测量误差。②低浓度样液差示法:用标准品制备浓度稍高于试样的参比溶液,将它放在光路上,打开光门,调节透光率至0%,然后换以空白溶剂,调节刻度至100%。此后测定样品的读数即可。
(4)多组分混合物的测定:当试样中有两种或两种以上的组分共存,可根据各组分的吸收光谱的重叠程度,选用不同的定量方法。如果混合物各组分的吸收峰互不干扰,这时可按单组分的测定方法,选择测定波长,分别测定各组分的含量;若各组分的吸收峰相互重叠,可采用解联立方程法、等吸收点法、双波长法等解决量中的干扰问题。
(5)利用摩尔吸光系数进行检测:①吸光系数:Beer定律的数学表达式为A=kbc,若溶液的浓度c以g/L为单位,b为光径以cm为单位,则常数K称为吸光系数,以a表示,其单位为升/(克.厘米)[L/(g.cm],A=kbc可写成A=abc。②摩尔吸光系数:公式A=kbc中的以为1mol/L,b为1cm时,则系数k称为摩尔吸光系数,以ε表示,单位为升/(摩尔.厘米)[L/(mol.cm)],A=kbc可写成A=εc。在实际工作中,不能直接用1mol/L这种高浓度的溶液测定吸光度,而是在稀释成适当浓度时测定吸光度进行运算。ε值与入射光波长、溶液的性质等因素有关。如NADH在260nm时ε为15000,写成ε260NADH=15×103;在340nm时ε为6220,写成ε340NADH=6.22×103。③比吸光系数:如公式A=kbc中的c是百分浓度(w/v)b为cm,则常数k可用E%表示,称为比吸光系数或百分吸光系数,A=kbc可写成A=E%bc。当待测物的化学结构是已知者可用ε值分析,若所测物的化学结构是未知的,则ε无法确定,此时用比吸光系数分析就很方便。a、ε和E常用作粗定量分析,主要用于定性分析。
近年来由于新的灵敏度高、选择性好的显色剂和掩蔽剂不断出现,一般不经分离过程即可直接比色测定。几乎所有的无机离子和有机物都可直接或间接用可见光及紫外光分光光度法进行定量测定。
2、原子吸收分光光度法 原子吸收光光度法是基于元素所产生的原子蒸气中,待测元素的基态原子,对所发射的特征谱线的吸收作用进行定量分析的一种技术。具有灵敏度高、选择性好、操作简便、分析速度快等优点,对大部分元素,其灵敏度约为10-8~10-10g/ml,是微量元素检测的一个十分有铲的方法之一。
(1)分析条件的选择
1)分析线:原子吸收法中常选择待测元素的共振作分析线,但并不是任何情况下都应使用共振线,例如As、Se、Hg的共振线在远紫外区,该区域火焰吸收强烈,不宜选用共振线作分析线。在选择分析线时,首先扫描空心阴极灯的发射光谱,然后喷入试样溶液,观察谱线的吸收和干扰情况,一般选用不受干扰且吸收最强的谱线作为分析线。常用元素分析线见表16-1。
表16-1 常用元素分析线
| 元素 | 分析线 | 元素 | 分析线 | 元素 | 分析线 |
| Al | 3093.3082 | Ca | 4227.2309 | Cd | 2288.3261 |
| Cu | 3248.3274 | Fe | 2483.3523 | Hg | 2537 |
| K | 7665.7699 | Mg | 2852.2796 | Na | 5890.3303 |
| Pb | 2167.2833 | Sn | 2246.2796 | Zm | 21393.3076 |
2)狭缝宽度的选择:适宜狭缝宽度可由实验确定:将试样喷入火焰,调节狭缝宽度,测定不同狭缝宽度时的吸光度,达到一定宽度后,吸光度趋于稳定,进一步增加狭缝宽度,当其他谱线或非吸收透过狭缝时,吸光度立即减小。不引起吸光度减小的最大狭缝宽度,就是最适宜的狭缝宽度。
3)原子化条件的选择:对于火焰原子化法,火焰的种类和燃助比的选择是很重要的。当燃气和助燃气选择好后,可通过下述方法选择燃助比:固定助燃气流量,改变燃气流量,测量标准溶液在不同燃助比时的吸光度,绘制吸光度-燃助比关系曲线,以确定最佳燃助比。
对于石墨炉原子化器的使用。应注意干燥是一个低温去溶剂的过程,可在稍低于溶剂沸点的温度下进行。灰化是为了破坏和去除试样基体,故在保证试样无明显损失的前提下,将试样加热到尽可能高的温度。原子化阶段应选择最大吸收信号的最低温度。总之,根据试样的性质确定各阶段所选定的温度与加热时间。
4)试样量的选择:火焰原子化法在一定范围内,喷入的试样量增加,原子吸光度增大,但在超过一定量后,由于试样不能完全有效地原子化及试液的冷却效应会使吸光度不再增大甚至有所下降。因此在保持一定的火焰条件下,测定吸光度随喷入试样量的增加达到最大吸光度时的喷雾量,就是适宜的试样量。石墨炉原子化一般固体取样0.1~10mg,液体取样量为1~50μl,主要依石墨管容器的大小而定。
(2)定量方法:常用的定量方法有标准曲线法、标准加入法和内标法。
1)标准曲线法:同紫外可见标准曲线法。但由于燃气流量和喷雾效率的变化,单色器波长的漂移等因素可导致样品测试条件与标准曲线测定条件不同,所以,在测定未知样品时,应随时对标准曲线进行检查,每次实验都要重新制作标准曲线。
2)标准加入法:在标准曲线法中,一般情况下要求标准溶液和未知溶液的组成保持一致。但在实际工作中不是总能做到的,采用标准加入法可以克服这个缺点。本法把未知试样溶液分成体积相同的若干份,留其中一份,其余分别加入不同量的标准样品,然后测定各溶液的吸光度,以吸光度为纵坐标,标准样品加入量为横坐标绘制标准曲线(图16-1)。由于未知样品中含待测组分,故直线不通过原点而是在吸光度高于原点的A0处与纵轴相交,且直线外推法使工作曲线延长交横轴处于B点,则OB所对应的浓度Cx就是未知试样中待测组分浓度。
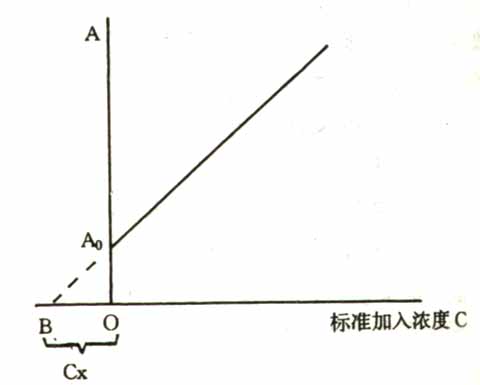
图16-1 标准加入法工作曲线
标准加入法的优点是能够更好地消除样品中其它成分对测定的影响。
3)内标法:在系列标准样品和未知样品中加入一定量试样中不存在的元素(内标元素),然后测得As和Ax,以As/Ax比值对标准样品中待测元素浓度C绘制标准曲线,再根据未加内标元素的试样A与加入内标元素的试样As比值(A/As)即可在标准曲线上求得试样中待测元素浓度。
本法要求内标元素应与待测元素有相近的物理和化学性质。此外,内标法只适用于双通道型原子吸收分光光度计。
(二)发射光谱分析法
1、荧光分析法 许多物质都是光致发光的,即它们可以吸收电磁辐射,然后又重新发射出相同或较长波长的辐射。光致发光最常见的类型是荧光(fluorescence)和磷光(phosphorescence)。利用荧光强度进行分析的方法,称为荧光法(fluorimetry)。在荧光分析中,待测物质分子成为激发态时所吸收的光称为激发光,处于激发态的分子回到基态时所产生的荧光称发射光。荧光法测定的是受光激发后所发射的荧光的强弱,而不是测定激发光的强弱。凡能产生荧光的化合的,均可采用荧光分析法进行定性或定量。
(1)荧光强度的影响因素
1)溶剂:增大溶剂的极性,将使π-π※跃迁的能量降低,荧光增强。在水、乙醇、环已烷等这些常用溶剂中常含有荧光杂质,影响测定,必须在使用前作净化处理。
2)荧光物质的浓度:对于某一荧光物质的稀溶液,在一定频率和一定强度的放射光Ⅰ。照射下,如果光被吸收的百分率不太大,且溶液的浓度很小,当溶液的厚度不变时,则它所发生的荧光强度F和该溶液的浓度C成正比,即F=φⅠ。ECL式中φ为荧效率。当荧光物质浓度高时,会发生分子间碰撞,使荧光效率降低。因为温度增高后使分子间碰撞次数增加,消耗分子的内部能量。
3)温度:大多数情况随温度升高时,荧光效率降低。因为温度增高后使分子间碰撞次数增加,消耗分子的内部能量。
4)溶液的PH值:当荧光物质本身为弱酸或弱碱时,溶液的pH值改变对溶液荧光强度产生影响较大,因为有些物质在离子状态时无荧光,而有些则相反,也有二者均有荧光,但荧光光谱有所不同。
(2)荧光定量分析法:荧光定量分析法通常有标准对比法和标准曲线法。操作和计算可参照比色法,但应注意,空白溶液的荧光强度F。往往不在零点,用上述两种方法时应先测定F,再从标准品Fs和试样Fx中减去F。后进行计算。
多组分混合物在荧光分析也可根据荧光峰相距情况采取不同的方法,如各组分荧光峰相距颇远,可分别在不同波长测定各个组分的荧光强度,然后直接求出各组分浓度。如果各组分荧光光谱相互重叠,利用荧光强度的加和性质,在适宜荧光波长处,测得混合物的荧光强度,再根据被测物质各自在适宜波长处的最大荧光强度,列出联立方程式求算各自的含量。
对较高浓度的荧光物质可用差示荧光法测定。
(3)荧光分析技术的应用:荧光分析法灵敏度高,选择性好、取样量少,因此已广泛应用于各领域,在临床生化检验方面可用于某些无机物与有机物的分析。
无机化合物能直接产生荧光并用于测定的为数不多,但与有机试剂络合后进行荧光分析的元素已达60余种,常见无机物的荧光测定见表16-2。
表16-2 常见无机物的荧光测定
| 元素 | 荧光试剂 | 激发波长(nm) | 荧光波长(nm) | 灵敏度(μg/ml) |
| Ag | 四氯荧光素 | 540 | 580 | 0.1 |
| Al | 桑色素 | 430 | 500 | 0.1 |
| Br | 荧光素 | 440 | 470 | 0.002 |
| Ca | 乙二醛-双-(4-羟苄基腙) | 453 | 523 | 0.0004 |
| Cl | 荧光素+AgNO3 | 254 | 505 | 0.002 |
| CN | 2',7'-双(乙酸基汞)荧光素 | 500 | 650 | 0.1 |
| Fe | 曙红+1,10-二氮杂非 | 540 | 580 | 0.1 |
| Pb | 曙红+1,10-二氮杂非 | 540 | 580 | 0.1 |
| Zn | 8-羟基喹啉 | 365 | 520 | 0.5 |
| F | 石榴茜互R-AI络合物 | 470 | 500 | 0.001 |
某些有机化合物的荧光测定应用较多,如糖类、胺类、甾族化合物、DNA与RNA、酶与辅酶、维生素等。常见有机化合物的荧光测定法见表16-3。
表16-3 常用有机化合物荧光测定法
| 待测物 | 试剂 | 激发波长(nm) | 荧光波长(nm) | 灵敏度(μg/ml) |
| 核酸 | 溴化乙啶 | 360-365 | 580-590 | 0.1 |
| 蛋白质 | 曙红y | 紫外 | 540 | 0.06 |
| 氨基酸 | 氧化酶等 | 315 | 425 | 0.01 |
| 肾上腺素 | 乙二胺 | 420 | 525 | 0.001 |
| NAD(P)H | 自身为荧光物质 | 340 | 450 | 10-6mol/L |
| ATP | 已糖激酶、6-磷酸葡萄糖脱氢酶、6-磷酸葡萄糖 | 340 | 450 | 2×10-6mol/L |
| 维生素A | 无水乙醇 | 345 | 490 | 0.001 |
2、火焰光度法火焰光度法是利用火焰中激发态原子回降至基态时发射的光谱强度进行含量分析的方法。它在仪器结构和分析操作上与火焰原子吸收法相似。
在火焰光度法中,试液和助燃气一起进入雾化室,雾化后喷入火焰,雾粒在火焰中蒸发和激发,激发态原子降落到低能态时发生光辐射,经单色器分光后到达检测器,然后由显示系统显示其发射光强度。
试样中的待测元素激发态原子的发射光强度I与该元素浓度C成正比关系,即I=aC。式中a为常数。a与试样的组成、蒸发和激发过程有关。
火焰光度法同样存在各种因素干扰,如供气压力,试样导入量、有机溶剂和无机酸的影响,以及金属元素间的相互作用等,某些干扰因素的消除方法同原子吸收法。对于金属离子间的相互作用可以下述方法予以消除:
(1)阳离子的干扰:第二阳离子的存在可使待测阳离子的电离作用降低而导致以元素形式存在居多,结果发射强度增大,这种现象称为阳离子增强效应。例如测定钙时有钾存在,钾可抑制钙的电离,干扰钙的测定。消除这种干扰的办法是在标准溶液及试样中加入本身易电离的金属如铯和锂。
(2)阴离子干扰:草酸根、磷酸根和硫酸根可与某些阳离子在火焰温度下形成仅能缓慢蒸发的化合物而抑制原子激发,结果导致待测元素发射强度降低。消除这种干扰的办法是用释放剂。释放剂的作用是同干扰阴离子牢固结合,使待测阳离子的激发行为不受干扰,或与待测阳离子形成更稳定而易挥发的配合物。故尽量避免使用磷酸、硫酸、草酸做试剂。
此外,应避免环境污染测试体系。使用的器皿应为塑料制品以防止玻璃器皿中金属溶出干扰测定。
火焰光度法通常采用的定量方法有标准曲线法、标准加入法和内标法。临床检验工作中前两种应用较多,而且测定血液或血清中钠和钾已成常规。应用火焰光度法测定某些元素的波长及检测限见表16-4。
表16-4 火焰光度法测定某些元素的波长与检测限
| 元素 | 测定波长(A) | 检测限(mg/L) | 元素 | 测定波长(A) | 检测限(mg/L) |
| Li | 6708 | 10-4 | Ca | 4227 | 3×10-3 |
| Na | 5890 | 10-4 | Sr | 4607 | 0.02 |
| K | 7665 | 10-3 | Ba | 4934 | 0.2 |
| Rb | 7800 | 0.05 | Mg | 3852 | 0.1 |
| Cs | 8521 | 1.0 |
散射光谱分析法主要测定光线通过溶液混悬颗粒后的光吸收或光散射程度的一类定量方法。测定过程与比色法类同,常用法为比浊法。但颗粒的大小和形状及悬液的稳定性对比浊结果有较大的影响,因此不能完全按比色法的规律进行测定,否则就会引起误差。
1、仪器和测定方法 由于测定仪器和方法的不同,比浊法又可分为散射测浑法(turbidimetry)和浊度测定法(nephelometry)二类。前者利用一般的光电比色计和分光光度计,其原理是利用光线通过混悬溶液时,由于颗粒的散射使通过的光线减弱,根据光线减弱的程度测定溶液中颗粒的浓度,所以,实际上可将散射测浑法看成是比色分析的一种特殊情况。后者则是直接测定混悬溶液中颗粒散射光的强度,由于一般光电比色计中光源和光电管在一直线上,无法测定散射光线的强度,需要特殊的浊度计,如激光比浊仪。测定方法可采用速率法或终点法进行。
速率散射比浊法是一种动力学测定方法,1977年由Seternbery首先用于免疫测定,在一定条件下,抗原和相应的抗体很快结合成抗原抗体免疫复合物颗粒,速率比浊法就是在一定时间内抗原抗体结合过程中,测定二者结合的最大反应速度,即反应达顶峰峰值。终点散射比浊法用于免疫测定时,在一定时间内,通常是抗原抗体反应达到平衡,复合物的浊度不再受时间的影响,但必须在聚合形成絮状沉淀之前进行浊度测定。
2、影响比浊法测定的因素比浊法的突出问题是颗粒的大小对浊度和浊度曲线有较大的影响。因此,在比浊法中必须力求作到:①混悬液中微粒的分散度也就是颗粒的大小应尽可能相同,并易重复。标准管和测定管中颗粒大小应力求一致。②混悬液在一定时间内,至少10分钟内应维持稳定,也就是颗粒应该不易相互聚集,变粗变大。为此,关键在于制备混悬液必须严格控制条件,一般应注意;①沉淀剂或抗体的浓度,一般情况下浊度随其浓度的增高而增大。②混匀方法和速度,一般而言,缓慢加入试剂,逐滴加入,不断摇匀,易产生粗颗粒沉淀;而迅速加入,迅速摇匀,易产生胶态溶液。③温度,温度升高可加快分子间的碰撞,常使某些在室温细小均匀的颗粒易变为粗大的絮状沉淀。④pH溶液,pH可影响沉淀的形成及颗粒的大小,如蛋白质、酶类,在其等电点pH值时最易形成颗粒并沉淀。⑤混悬液的稳定性和测定时间,大多数混悬液随放置时间的延长颗粒变粗而沉淀,吸光度下降,因此应及时比浊。如出现沉淀太快,可以加入保护性胶体,如聚乙烯吡咯烷酮、表面活性剂等,但应注意加入后可能会引起颗粒及光学性质的变化。⑥其它电解质和非电解质存在的干扰。由此可见,比浊法易受外界各种因素的影响,因此在建立一种比浊测定方法时,必须认真探索其反应规律,力求控制各种影响因素以克服比浊法重复性和准确性较差的缺点。
3、比浊法的应用目前在临床生化检验中使用最多的比浊法是免疫比浊法,如免疫球蛋白、载脂蛋白和补体等项目均已大部分用免疫比浊法进行快速定量。
早在1838年Libby等人把比浊法测定就应用到抗原抗体反应上。所谓免疫比浊法是利用抗原和抗体的特异性结合形成复合物,通过测定复合物形成量的多少,对抗原或抗体进行定量的方法。在介质溶液中形成复合物需要一定的条件,包括:①要有特异性抗体。作为组织或体液中蛋白质种类相当多,若要快速特异测定,就需要有单价特异抗体,也就是说,某一种蛋白有其特异抗体才能与该抗原结合,形成免疫复合物,再定量。若抗体不纯或混有另一种或两种少量抗体,这种免疫复合物就不是单一复合物而是大杂烩,结果偏高。②抗原抗体的比例要适当。因免疫复合物的形成有三个阶段,第一阶段是初步形成抗原抗体二元复合物;第二阶段是复合物交联成大的网络状结构;第三阶段是复合物聚合产生絮状沉淀。只有在抗原与抗体等价时即无过剩抗体,此时,复合物的结合和解离处在平衡状态,其混浊程度达高峰,在抗体过量时,随抗原量的增加而复合物的形成也增加,成正比关系,其测定只能在以应曲线的左侧进行。同时,抗原也不能过量,因为抗原过量,则复合物减少,光散射或光吸收就减少,检测结果偏低。③溶液介质适宜,一般要求溶液中有非离子性亲水多聚体促进免疫复合的形成,如聚乙二醇6000等,溶液pH以6.5~8.0之间为宜,离子强度大比小易形成复合物,对离子的种类也有一定的要求。
在免疫比浊过程中,由于抗原与抗体结合有三个阶段,从而导致吸光度与浓度之间不呈线性关系,一般是三次程曲线关系。如果要将抗原与抗体两个变量之间的变动特征恰当地反映出来,需要经三次程拟合成近似直线化的曲线方程,再进行运算。方法可采用终点法和速率法,用五个不同浓度进行定标,经三次曲线方程求出一条能反映真实情况的浓度与吸光度的关系曲线方程。作为定量的工作曲线。
| 关于“临床生物化学/光谱分析的常用方法”的留言: | |
|
目前暂无留言 | |
| 添加留言 | |